Abr
24
Química: Alquimia y todavía más.
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Química ~
Clasificado en Química ~
 Comments (2)
Comments (2)

El 16 de febrero de 1785 Antoine-Laurent de Lavoisier sintetiza agua a base de hidrógeno y oxígeno. Lavoisier fue un químico francés que junto a su esposa, la científica Marie Lavoisier, realizó grandes contribuciones a la química. Se le considera el “padre de la química” por sus detallados estudios, entre otros: el estudio del aire, el fenómeno de la respiración animal y su relación con los procesos de oxidación, el análisis del agua y el uso de la balanza para establecer relaciones cuantitativas en las reacciones químicas estableciendo su famosa Ley de conservación de la masa



Antoine-Laurent Lavoisier (1743-1794) fue un financiero. Estableció un sistema de pesos y medidas que condujo al sistema métrico, vivió los primeros momentos turbulentos de la Revolución Francesa y fue pionero en la agricultura científica. Se casó con una jovencita de catorce años y fue decapitado durante el Terror. Se le ha llamado padre de la química moderna y, a lo largo de su atareada vida, sacó a Europa de las épocas oscuras de esta ciencia.
![[8426-004-BDD1097F.jpg]](http://2.bp.blogspot.com/_y4MCc7YOA-A/SS4Np8kKtFI/AAAAAAAAAA4/U6Zj6HajIec/s1600/8426-004-BDD1097F.jpg)
Una de las primeras aportaciones de Lavoisier surgió cuando éste hizo el experimento de hervir agua durante largos períodos de tiempo. En la Europa del siglo XVIII muchos científicos creían en la transmutación. Pensaban, por ejemplo, que el agua podía transmutarse en tierra, entre otras cosas. Entre las pruebas, la principal consistía en hervir agua en una cazuela: en la superficie interior se formaban residuos sólidos. Algunos científicos proclamaron que esto se debía a que el agua se convertía en un nuevo elemento. Robert Boyle, el gran físico y químico británico del siglo XVII que llegó al apogeo de su actividad científica cien años antes que Lavoisier, creía en la transmutación. Después de observar cómo crecían las plantas absorbiendo agua, llegó a la conclusión – al igual que muchos antes que él – de que el agua podía transformarse en hojas, flores y bayas. Según dice el químico Harold Goldwhite, de la State University de California, en Los Ángeles, “ Boyle fue un activo alquimista ”.
Boyle
El mérito que tuvieron aquellos pioneros…con tan pocos medios, agranda aún más los enormes logros y los descubrimientos que hicieron.
Lavoisier observó que el peso era la clave y que las mediciones eran fundamentales. Puso agua destilada en un hervidor especial en forma de tetera llamado pelícano, un recipiente cerrado con una tapa esférica que tomaba el vapor del agua y lo devolvía a la base del recipiente por dos tubos parecidos a unas asas. Hirvió el agua durante 101 días y encontró un residuo considerable. Pesó l agua, el residuo y el pelícano. El agua pesaba exactamente lo mismo. El pelícano pesaba algo menos, una cantidad exactamente igual al peso del residuo. Por lo tanto, el residuo no era producto de una transmutación, sino parte del recipiente: vidrio disuelto, sílice y otras sustancias.
Sep
23
¡El carbono! elemento esencial para la vida
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Química ~
Clasificado en Química ~
 Comments (9)
Comments (9)
¿Por qué hay vida en el Universo?

La Tierra es el mayor de los planetas interiores y se creó como todos los planetas restantes del Sistema Solar, hace aproximadamente 4.6 miles de millones de años. La Tierra primigenia se formó por la colisión y fusión de fragmentos de rocas más pequeños, de los denominados planetesimales.
En la Tierra primigenia se encontraban presentes todos los elementos esenciales para la vida. Sobre la base del Carbono y con la ayuda de otros, la presencia de una atmósfera, la radiación del Sol que daba luz y calor al planeta, los océanos y otros muchos ingredientes (como la distancia desde la Tierra al Sol) hicieron posible el surgir de aquella primera célula replicante que dió comienzo a la fascinante aventura de la vida.
No pocas veces nos hemos podido preguntar que, dadas las condiciones que imperaban en la Tierra hace cuatro mil millones de años, ¿que probabilidades había de que surgiera la vida? Lo más fácil sería responder que la Vida era inevitable, como lo demuestra el simple hecho de que nosotros estemos aquí. Es obvio que la vida sí se inicio y que nuestra presencia la testifica pero, ¿tenía que iniciarse? O, preguntado de otra manera, ¿era inevitable la emergencia de la vida a partir de un caldo químico o cualquier otra cosa, contando con millones de años?
Nadie conoce la respuesta a esa pregunta. El origen de la vida puede haber sido también, una extraordinaria “carambola”, un accidente químico de enorme improbabilidad, un suceso tan poco probable que nunca sucedería dos veces en todo el universo. O quizá haya sido tan poco notable y tan predeterminada como la formación de los cristales de sal. ¿Cómo podemos saber que explicación es la correcta?
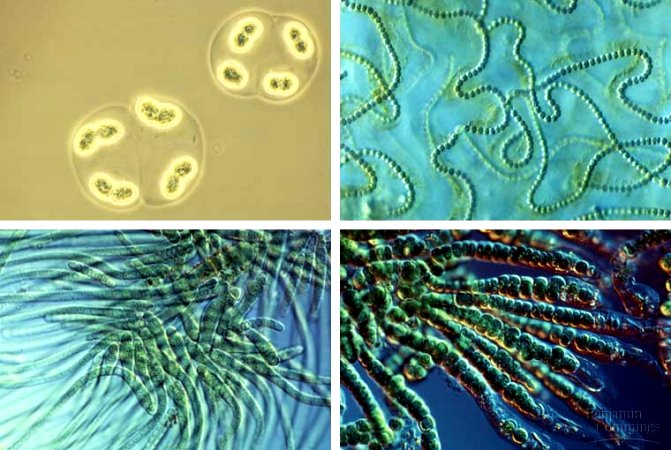
En algún momento del pasado de la Tierra, estimado en aproximadamente 2.500 – 3.500 millones de años, tuvo lugar lo que denominamos revolución oxigénica, durante la cual las cianobacterias produjeron tanto oxígeno que la atmósfera y los océanos quedaron literalmente saturados de este nuevo compuesto químico. Tal producción de oxígeno afectó drásticamente a la biósfera del planeta.
Antes de la revolución oxigénica, pocos organismos estaban adaptados para vivir en presencia de oxígeno abundante; las moléculas de oxígeno actuaban como un veneno, reaccionando con las moléculas orgánicas complejas y degradándolas. Debido a esto, la mayor parte de la vida existente en ese momento debió quedar exterminada; las cianobacterias serían responsables de una gran extinción masiva.
Sabemos que la vida terrestre está basada en algunas moléculas muy complicadas con estructuras cuidadosamente elaboradas, incluso en los organismos simples, el ADN contiene millones de átomos. La secuencia exacta de los átomos es crucial. No se puede tener una secuencia arbitraria porque el ADN es un manual de instrucciones para conseguir un organismo y, si cambiamos algunos átomos se pondrá en peligro toda la estructura del organimo.Claro que pensar en manejar aminoácidos al azar y obtener la secuencia correcta para formar una molécula de proteína por accidente…es complicado. Las probabilidades en contra de producir las proteínas por puro azar son del orden de 1040000 contra 1 seguido de cuarenta mil ceros, cuya escritura completa necesitaría de muchas hojas en blanco para ser reflejada. Fred Hoyle, siempre hacía esta comparación: “Un ensamblaje espontáneo de la vida sería lo mismo y tendría las mismas probabilidades que si un Tornado barriera un depósito de chatarra y surgiera un Boeing 747 listo para funcionar.
La inmensa complejidad que el misterio de la vida conlleva, nos ha llevado a pensar en la posibilidad extraterrestre y en otros múltiples modelos que, de alguna manera, nos pudieran aclarar ese origen que tan afanosamente buscamos sin éxito…de momento. Algunas personas sienten que algo tan básico como nuestra propia existencia no puede deberse a un azar químico, y que barrer el problema bajo la alfombra con la palabra “accidente” es una manera de escabullirse. A veces se cita el principio de mediocridad: no hay nada especial o excepcional en nuestro lugar en el Universo. La Tierra parece un planetas típico alrededor de una estrella típica en una galaxia típica. Si eso es así (que lo), ¿por qué no sería, también típica la vida en la Tierra?

Pero, a todo esto, por mucho que hayamos podido elucubrar sobre el tema, lo ciert0 es que, no podemos contestar la pregunta: ¿Por qué y cómo realmente, llegamos aquí, y, si también podemos estar en otros mundos?
La enorme variedad de formas, colores, comportamientos, composición…, que acompaña a los objetos, incluidos los vivientes, sería una consecuencia de la riqueza en la información que soportan las moléculas (y sus agregados) que forman parte de dichos objetos. Ello explicaría que las moléculas de la vida sean en general de grandes dimensiones (macromoléculas). La inmensa mayoría de ellas contiene carbono. Debido a su tetra-valencia y a la gran capacidad que posee dicho átomo para unirse consigo mismo, dichas moléculas pueden considerarse como un esqueleto formado por cadenas de esos átomos.
El carbono no es el único átomo con capacidad para formar los citados esqueletos. Próximos al carbono en la tabla periódica, el silicio, fósforo y boro comparten con dicho átomo esa característica, si bien en un grado mucho menor.
Refiriéndonos al silicio, señalaremos que las “moléculas” que dicho átomo forma con el oxígeno y otros átomos, generalmente metálicos poseyendo gran nivel de información, difieren en varios aspectos de las moléculas orgánicas, es decir, de las que poseen un esqueleto de átomos de carbono.

El silicio púede configurar muchas formas y, no creo que entre ellas se puedan encontrar las vivientes, ya que, el átomo de silicio no llega a tener las amplias propiedades que tiene el Carbono. Sin embargo, no son pocos los que opinan que puede existir alguna clase de vida basada en el silicio y, desde luego, aunque no lo crea probable tampoco tengo conocimientos suficientes para poder negarlo. ¿Quién sabe lo que por ahí fuera pueda existir en esos mundos perdidos en la lejanía del espacio?
El mundo de los silicatos es de una gran diversidad, existiendo centenares de especies minero-lógicas. Esas diferencias se refieren fundamentalmente a que el enlace químico en el caso de las moléculas orgánicas es covalente, y cuando se forma la sustancia correspondiente (cuatrillones de moléculas) o es un líquido, como es el caso de los aceites, o bien un sólido que funde fácilmente. Entre las moléculas que lo forman se ejercen unas fuerzas, llamadas de Van der Waals, que pueden considerarse como residuales de las fuerzas electromagnéticas, algo más débiles que éstas. En cambio, en los silicatos sólidos (como en el caso del topacio) el enlace covalente o iónico no se limita a una molécula, sino que se extiende en el espacio ocupado por el sólido, resultando un entramado particularmente fuerte.

Sep
21
Hablemos de cuerpos
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Química ~
Clasificado en Química ~
 Comments (0)
Comments (0)
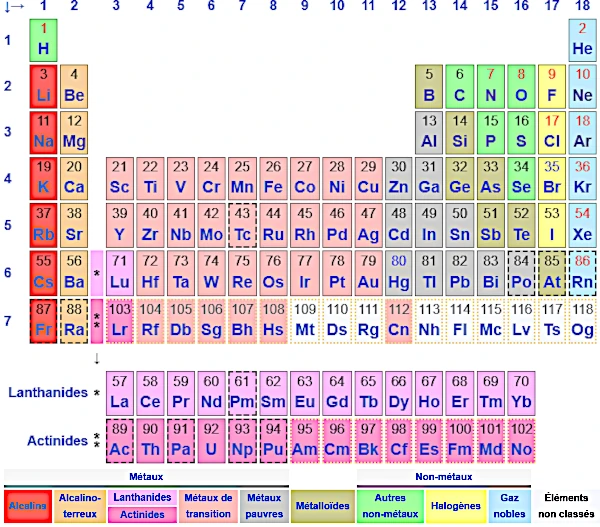
Me referiré en primer lugar a los que constituyen nuestro entorno ordinario, que sería todo el entorno que abarca nuestro planeta. En segundo lugar considerare los demás cuerpos y objetos del Universo. El análisis de muestras de esos diversos cuerpos ha puesto de manifiesto que, en función de la composición, los cuerpos pueden ser simples y compuestos. Los primeros son, precisamente, los llamados elementos químicos, a las que el insigne Lavoisier (conocido como padre de la Química), consideró como el último término a que se llega mediante la aplicación del análisis químico.

Hoy sabemos que son colectividades de átomos isotópicos.

La mayoría de ellos son sólidos y se encuentran en la Naturaleza (nuestro entorno terráqueo) en estado libre o en combinación química con otros elementos, formando los diversos minerales.

En un principio, todos los organismos vivos fueron clasificados como animales o plantas y, en este segundo grupo, fueron incluidos una variedad de seres, tales como hongos, bacterias y protistas. Con el paso del tiempo y el desarrollo de nuevas técnicas taxonómicas, los seres vivos pasaron a ser clasificados según sus características en 5 reinos:

Animalia, Fungi, Protista, Monera y Plantae, aunque también hay quién los clasifica en 6 separando el conocido reino Monera entre Arquea y Bacteria. Esta es la clasificación actualmente reconocida y el reino Plantae es el que incluye todas las plantas.

Aunque no todas las personas conocen la definición de la palabra animal, casi todos saben diferenciarlos de otros seres vivos. El reino Animalia o animal comprende todos aquellos organismos a los que se denomina animales, seres reconocibles por las características de sus movimientos y sus reacciones frente al entorno. Cabe destacar que a los animales también se les conoce como metazoos.

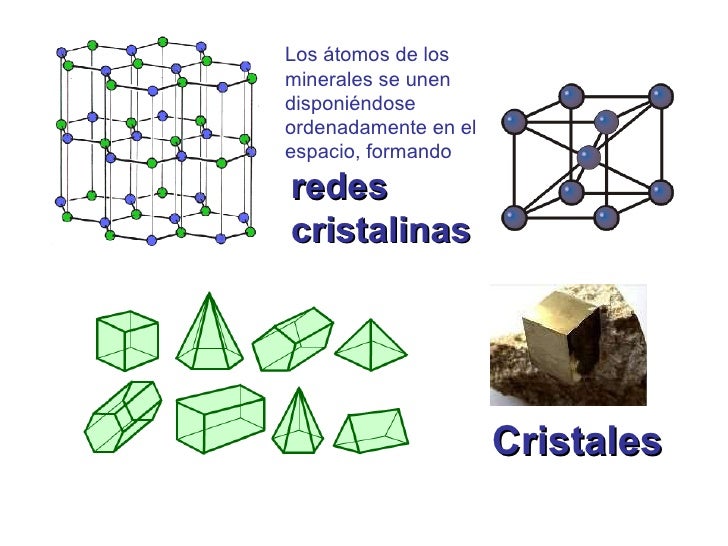
La ordenación de los iones en las redes se manifiesta externamente en multitud de formas y colores. No obstante, debo señalar que, aun siendo abundante esta variedad, no es tan rica como la que corresponde a los cuerpos vivos, tanto animales como vegetales. La explicación se basa en que el número de especímenes moleculares y su complejidad son mucho mayores que en el reino inorgánico.
Sería conveniente, salir al paso de una posible interpretación errónea. Me refiero a que pudiera pensarse que los reinos que acabamos de mencionar constituyen clases disyuntas, esto es, sin conexión mutua. Y no lo digo porque esté considerando el hecho de que el carbono forma compuestos inorgánicos y orgánicos (lo que también hace el silicio), sino porque haya existido, y aún pueda existir, una conclusión, mejor conexión evolutiva del mundo inorgánico y el viviente que no se puede descartar, de hecho, yo particularmente, estoy seguro de ello. Estamos totalmente conectados con los ríos, las montañas y los valles, con la tierra que pisamos, el aire que respiramos y con todo el resto del Universo del que formamos parte.

La teoría de Cairos Swith considera que el eslabón entre ambos mundos se halla localizado en los microcristales de arcilla. Mi teoría particular es que no hay eslabón perdido en dicha conexión, sino que es el tiempo el que pone, en cada momento, una u otra materia en uno u otro lugar. Ahora, nos ha tocado estar aquí como ser complejo, pensante y sensitivo. El eón que viene nos puede colocar formando parte de un enorme árbol, de un monte, o, simplemente estar reposando como fina arena en el lecho de un río. Sin dudarlo, J.M.y P. formarán parte de un hermoso jardín perfumado y lleno de aromas que la brisa regalará a los que pasen cerca de allí.

El granito, por ejemplo, consiste básicamente en una mezcla de tres cuerpos compuestos: cuarzo, mica y feldespato. ¿Quién puede decir hoy lo que seremos mañana?
En todos los cuerpos que hemos estado considerando hasta ahora, las moléculas, los átomos o los iones se hallan situados en los nudos de la correspondiente red, así que, los electrones de esos individuos se encuentran también localizados en el entorno inmediato de esos lugares. Podríamos decir que la densidad electrónica es una función periódica espacial, lo que significa que al recorrer la red siguiendo una determinada dirección irían apareciendo altibajos, es decir, crestas y valles de la densidad electrónica.

La estructura de los cuerpos metálicos, así como las aleaciones, merecen una consideración especial. La estructura de los metales y aleaciones difiere de la de los demás cuerpos en un aspecto muy importante que consideraré a continuación.
Me refiero a que en los cuerpos metálicos existe una deslocalización de los electrones que están menos fuertemente enlazados en los correspondientes núcleos, es decir, de los electrones de valencia.

Vamos a precisar un poco. Supongamos, para fijar las ideas, que tenemos un trozo de plata metálica pura. En los nudos de la red correspondientes los átomos han perdido su electrón de valencia, pero ocurre que cada uno de estos electrones forma una colectividad que se halla desparramada o dispersa por todo el sólido. Una primera imagen de esta situación fue establecida por el gran físico italiano Enrico Fermi, por lo que se habla de un gas electrónico, llamado también de Fermi, que llenaría los espacios libres, es decir, no ocupados por los iones metálicos.


Moléculas, sustancias, cuerpos
Este gas electrónico es el responsable de las propiedades metálicas, tales como el brillo, conductibilidades eléctrica y térmica, etc. La aplicación de la mecánica cuántica a la descripción del estado metálico conduce a la obtención del mapa de la densidad electrónica, o, como decía antes, a las características de la información correspondiente.
Sin entrar en detalles que desviarían nuestra atención hacia otros conceptos fuera de los límites de lo que ahora estoy pretendiendo, utilizaré el mismo lenguaje que para las estructuras de núcleos y átomos.
Recordemos que en la sociedad de los nucleones y electrones existen las relaciones verticales y las de estratificación, que se manifiestan en las capas y subcapas. En el caso de los metales tendríamos una colectividad de núcleos, arropados con sus capas cerradas, ocupando los nudos de la red; únicamente los electrones de valencia de cada átomo forman la colectividad del gas electrónico.
![]()
La pregunta que nos debemos hacer es: ¿estos electrones, en número igual, por lo menos, al de los átomos, se hallan estratificados? La respuesta es que sí. Existe una estratificación de estos electrones en las llamadas bandas. El concepto de banda energética resulta de la consideración simultánea de dos aspectos: la cuantización energética ( o la estratificación de los niveles energéticos en los átomos) y el grandísimo número de electrones existentes. Este colectivo no podría ubicarse en un número finito y escaso de niveles. Esta dificultad queda soslayada si se admite que cada uno de esos niveles atómicos de los N átomos que forman el cuerpo se funde en otros tantos niveles de cierta anchura donde ya pueden alojarse los electrones disponibles.
Esa fusión de los niveles atómicos da lugar a las bandas. Esta imagen equivaldría a considerar un metal como un átomo gigante en el que los niveles energéticos poseyeran una anchura finita.

En cuanto a la información que puede soportar un metal, podríamos señalar que sería parecida a la del correspondiente átomo, pero mucha más extendida espacialmente. Una información puntual, la del átomo, daría paso a otra espacial, si bien vendría a ser una mera repetición periódica de aquella.
¿Y los cuerpos que pueblan el resto del Universo?
Cuando un cuerpo sobrepasa unas determinadas dimensiones, aparece algo que conocemos como fuerza gravitatoria y que se deja sentir en la forma que todos conocemos y, que da lugar, primeramente a la fusión de los diversos materiales que forman los cuerpos.
Así, por ejemplo, en el cuerpo que llamamos Tierra, la presión crece con la profundidad, por lo que, a partir de un determinado valor de ésta, aparece el estado líquido y con él una estratificación que trata de establecer el equilibrio hidrostático.

Dentro de nuestro sistema planetario se distinguen los planetas rocosos, hasta Marte y meteoritos inclusive, y el resto de ellos, desde Júpiter en adelante, incluido este. Estos últimos difieren esencialmente de los primeros en su composición. Recuérdese que la de Júpiter es mucho más simple que la de los planetas rocosos. Consta fundamentalmente de hidrógeno, helio, agua, amoniaco y metano, con un núcleo rocoso en su interior. El hidrógeno que rodea a este núcleo se encuentra en forma de hidrógeno atómico sólido*
También la composición del Sol (y todas las estrellas que brillan) es más simple que la de los planetas rocosos, su estado físico es el de plasma y su contenido está reducido (mayormente) a hidrógeno y helio. Mas variedad de materiales existe en las estrellas supernovas, donde el primitivo hidrógeno ha evolucionado de la manera que expliqué en otra parte de este trabajo.
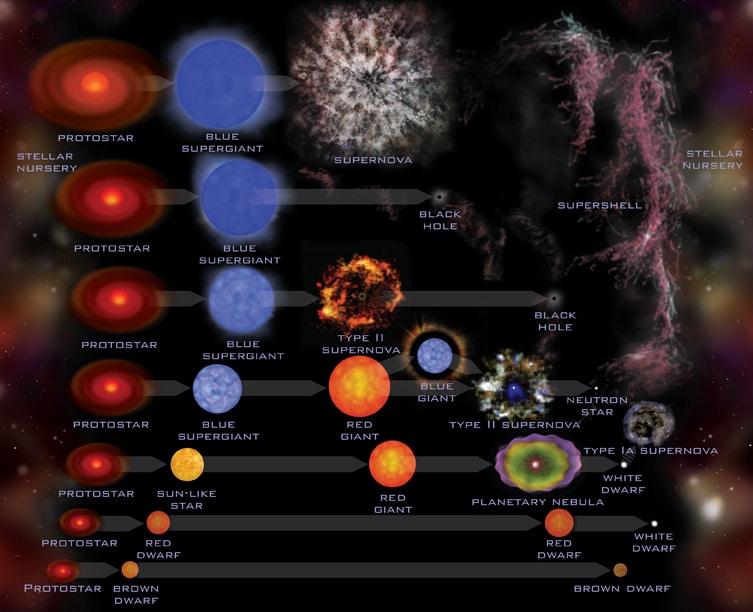
En cuanto a los derechos de la evolución estelar, enanas blancas, estrellas de neutrones y agujeros negros, señalaré que la composición de la primera es sencilla en cuanto al numero de “elementos” constituyentes; la segunda ya lo indica su propio nombre, constan de nucleones, particularmente neutrones que están fuertemente empaquetados (muy juntos) por la gravedad. Una estrella de neutrones puede tener una densidad superior a la del agua, en millones de veces y del mismo orden que la de los núcleos atómicos. El agujero negro, es un fenómeno aparte, su inmensa fuerza gravitatoria es tal que, ni la luz puede escapar de ella, es decir, su velocidad de escape es superior a 300.000 km/s, y, como según la relatividad, nada es en nuestro Universo, superior en velocidad, a la luz, resulta que nada podrá escapar de un agujero negro.
Allí dentro, en el interior del agujero negro, no existen ni el tiempo ni el espacio, es como un objeto que estando en nuestro Universo (deja sentir su fuerza gravitatoria y engulle estrellas), al mismo tiempo, no está aquí.
Desde el comienzo de este trabajo estoy tratando de relacionar el Universo, la materia y la consciencia, es por ello que me he entrenido en dar tantas explicaciones que, para no resultar pesado, he amenizado con alguna que otra historia, noticia o comentario.
Ha sido un largo recorrido por las profundidades de la materia vista desde distintas perspectivas, y, en ella, estamos nosotros incluidos, con una adicional: El pensamiento, la racionalidad: el Ser.
Emilio Silvera V.
En todo el Universo, siempre es lo mismo, rigen las mismas leyes, las mismas fuerzas y está presente la misma materia. Sin embargo y aunque no la podemos ver por ninguna parte, la mayoría postula la existencia de la “materia oscura” que, la inventó un cosmólogo cuando no podía explicar el movimiento de las galaxias, y, todos sin excepción se agarraron a la idea como el que se ahoga a un hierro candente.
El Físico y premio Nobel Martinus J. G. Veltman, lo define muy bien:
“La materia oscura es la alfombra bajo la cual, los cosmólogos, barren su ignorancia.”
| Quarks
Nucleones Núcleos Átomos Moléculas Sustancias Cuerpos Planetas ( Vida ) Estrellas Galaxias Cúmulos de Galaxias UNIVERSO |
Al final todo se reduce a Quarks y Leptones que son las partículas que conforman toda la materia conocida esté viva o inanimada. Claro que, cuando hablamos de “materia inerte” lo tendríamos que hacer con cierta precaución, ya que, la Vida… ¿No surgió de la “materia inerte” evolucionada?
Emilio Silvera V.
May
3
Cosas que debemos saber I
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Química ~
Clasificado en Química ~
 Comments (1)
Comments (1)


En una supernova, en orden decreciente tenemos la secuencia de núcleos H, He, O, C, N, Fe, que coincide bastante bien con una ordenación en la tabla periódica que es:
H, He, (Li, Be, B) C, N, O… Fe
¿Apreciáis la maravilla? Las estrellas brillan en el cielo para hacer posible que nosotros estemos aquí descubriendo los enigmas del universo y… de la vida inteligente.
Pero está claro que todo el proceso estelar evolutivo inorgánico nos condujo desde el simple gas y polvo cósmico a la formación de estrellas y nebulosas solares hasta los planetas, la Tierra en particular, en cuyo medio ígneo describimos la formación de las estructuras de los silicatos, desplegándose con ello una enorme diversidad de composiciones, formas y colores, asistiéndose, por primera vez en la historia de la materia, a unas manifestaciones que contrastan con las que hemos mencionado en relación al proceso de las estrellas.
Desde el punto de vista del orden es la primera vez que nos encontramos con objetos de tamaño comparables al nuestro, en los que la ordenación de sus constituyentes es el rasgo más característico.
Mar
28
2011, Año Internacional de la mujer científica y de la Química
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Química ~
Clasificado en Química ~
 Comments (8)
Comments (8)
Sí, queridos amigos, el año 2011 fue el elegido como Año Internacional de la mujer científica, ya que, se cumplieron 100 años desde que, Marie Curie obtuviera el Nobel de Química, y, en ella se ha querido simbolizar un homenaje a todas las mujeres que a lo largo de la historia de la Ciencia, han contribuido en uno u otro campo, al saber del mundo.
Hacer aquí una mención pormenorizada de todas ellas, es imposible, y, como el modelo elegido a sido Marie Curie, aquí os dejo un reflejo de quien fue con datos tomados de diferentes fuentes:
“MARIE CURIE: LA GRAN APORTACIÓN CIENTÍFICA DE LA MUJER
Marie Curie, también conocida como Maria Sklodowska-Curie, fue una química y física polaca, posteriormente nacionalizada francesa. Pionera en el campo de la radioactividad, fue la primera persona en recibir dos premios Nobel (premio Nobel de Física en 1903 y de Química en 1911) y la primera mujer en ser profesora en la Universidad de París.
Todo empezó con la elección del tema de su tesis doctoral. Tras analizarlo con su marido (el físico Pierre Curie), ambos decidieron centrarse en los trabajos del físico Henri Becquerel (al que se le concedió el Nobel de Física, junto con el matrimonio Curie, en 1903), que había descubierto que las sales de uranio transmitían unos rayos de naturaleza desconocida. Este trabajo estaba relacionado con el reciente descubrimiento de los rayos X por parte del físico Wilhelm Röntgen. Marie Curie se interesó por estos trabajos y, con la ayuda de su esposo, decidió investigar la naturaleza de las radiaciones que producían las sales de uranio.
- “La mejor vida no es la más larga, sino la más rica en buenas acciones.”
- “La vida no es fácil, para ninguno de nosotros. Pero… ¡qué importa! Hay que perseverar y, sobre todo, tener confianza en uno mismo. Hay que sentirse dotado para realizar alguna cosa y que esa cosa hay que alcanzarla, cueste lo que cueste.”
















 Totales: 89.070.270
Totales: 89.070.270 Conectados: 23
Conectados: 23























