May
1
Lo cierto es que…, nunca dejáremos de hacernos preguntas.
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (6)
Comments (6)

Aunque es cierto que “sobre gustos no hay nada escrito”, los humanos nos sentimos más a gusto con las caras más simétricas. En la cultura popular, y salvo alguna rara excepción, las caras asimétricas están relacionadas con la maldad. Los biólogos encontraron rápidamente una explicación evolutiva: los individuos más evolucionados pueden mantener sus formas simétricas inclusive cuando están expuestos al estrés y las enfermedades. Es decir, cuando las partes del cuerpo que tienden a la simetría no lo son, costará más pasar esos genes porque será rechazado por potenciales parejas. De esta manera la evolución distingue a la simetría como una característica valiosa.
David (1501-1504), de Miguel Ángel, Galería de la Academia de Florencia.
El desnudo de una figura humana presenta una simetría bilateral casi perfecta. Ciertamente, parte del atractivo del mismo, tanto en la realidad como en el arte, reside en la identificación de los lados derecho e izquierdo del cuerpo mediante mediante una simetría especular. La figura femenina raramente presenta asimetrías. La asimetría de un varón se rompe solamente por la curiosa circunstancia de que su testículo izquierdo cuelga más bajo que el derecho.
presenta una simetría bilateral casi perfecta. Ciertamente, parte del atractivo del mismo, tanto en la realidad como en el arte, reside en la identificación de los lados derecho e izquierdo del cuerpo mediante mediante una simetría especular. La figura femenina raramente presenta asimetrías. La asimetría de un varón se rompe solamente por la curiosa circunstancia de que su testículo izquierdo cuelga más bajo que el derecho.

Venus (1532), de Lucas Cranach el Viejo, Städelsches Kunstinstitut, Fráncfort del Meno, censurada por el Metro de Londres en 2008.
(1532), de Lucas Cranach el Viejo, Städelsches Kunstinstitut, Fráncfort del Meno, censurada por el Metro de Londres en 2008.
Evidentemente, cada cuerpo, considerado de forma individual, puede tener otras desviaciones menores de su simetría: un hombro más alto que otro, un pecho mayor que su pareja, una ligera desviación de la columna, una peca o un antojo en un costado…, pero tales anomalías, en su mayor parte, pueden encontrarse tanto a un lado como al otro.
otras desviaciones menores de su simetría: un hombro más alto que otro, un pecho mayor que su pareja, una ligera desviación de la columna, una peca o un antojo en un costado…, pero tales anomalías, en su mayor parte, pueden encontrarse tanto a un lado como al otro.

La simetría bilateral se mantiene en el interior del cuerpo, en especial en los músculos y en el esqueleto, pero queda rota por la disposición fuertemente asimétrica de algunos órganos. El corazón, el estómago y el páncreas están desviados hacia la izquierda; el hígado y el apéndice, hacia la derecha. El pulmón derecho es mayor que el izquierdo. Los retorcimientos y vueltas de los intestinos son completamente asimétricos. El cordón umbilical humano, una magnifica hélice triple formada por dos arterias y una vena, puede enrollarse en cualquiera de los dos sentidos.
en los músculos y en el esqueleto, pero queda rota por la disposición fuertemente asimétrica de algunos órganos. El corazón, el estómago y el páncreas están desviados hacia la izquierda; el hígado y el apéndice, hacia la derecha. El pulmón derecho es mayor que el izquierdo. Los retorcimientos y vueltas de los intestinos son completamente asimétricos. El cordón umbilical humano, una magnifica hélice triple formada por dos arterias y una vena, puede enrollarse en cualquiera de los dos sentidos.

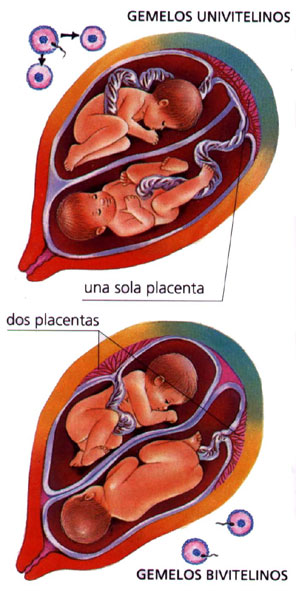
Los mellizos que se desarrollan por la fecundación simultánea de dos óvulos separados, pueden tener detalles asimétricos en un sentido en uno de ellos, y en el contrario en el otro, pero esto no ocurre con mayor frecuencia que la que cabría esperar como fruto del azar. Es una creencia generalizada que los gemelos (formados a partir de un único óvulo, que se divide inmediatamente después de la fecundación) tiene una marcada tendencia a aparentar imágenes especulares recíprocas. Por desgracia, las estadísticas al respecto son confusas y muchos expertos creen que los gemelos idénticos no se presentan como imágenes especulares uno de otro en mayor medida que cualquier otro tipo de hermanos.
especulares recíprocas. Por desgracia, las estadísticas al respecto son confusas y muchos expertos creen que los gemelos idénticos no se presentan como imágenes especulares uno de otro en mayor medida que cualquier otro tipo de hermanos.
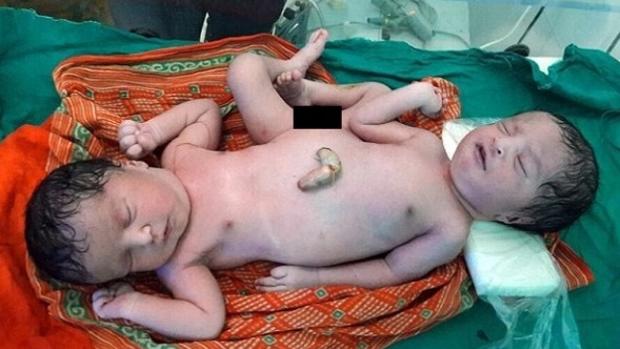
En el caso de gemelos siameses (gemelos idénticos, unidos uno a otro a causa de un a partición tardía e incompleta del óvulo), el tema no ofrece duda alguna. Son exactamente enantiomorfos en casi todos los detalles: si uno es diestro, el otro es zurdo; si uno tiene el remolino del pelo que va en el sentido de las agujas del reloj, el de su hermano/hermana irá en el sentido contrario. Diferencias en los oídos, los dientes…, aparecen en ambos como imágenes especulares unas respecto de otras (hasta en eso es perfecta la Naturaleza). Las huellas dactilares o de la palma de la mano derecha de uno serán muy parecidas a las correspondientes a la mano izquierda del otro.
especulares unas respecto de otras (hasta en eso es perfecta la Naturaleza). Las huellas dactilares o de la palma de la mano derecha de uno serán muy parecidas a las correspondientes a la mano izquierda del otro.
Todavía más: un gemelo siamés tendrá “vísceras transpuestas”; sus órganos internos estarán colocados de manera inversa, el corazón a la derecha, el hígado a la izquierda. Esta transposición de órganos, o inverse situs, como se denomina a veces, se da siempre en cualquier par de gemelos siameses, pero puede aparecer también en personas no incluidas en estas circunstancias.
no incluidas en estas circunstancias.

Merece la pena hacer notar que Lewis Carroll, en A través del espejo (Alianza Editorial, 1990), pretende tomar los gemelos idénticos Tararí y Tarará como imágenes especulares uno de otro. Cuando los hermanos Tara ofrecen enlazar sus manos con Alicia, uno de ellos alarga su mano derecha; el otro la izquierda. Si observamos detenidamente las ilustraciones de Tenniel, especialmente la que muestra los dos gemelos uno frente a otro, vestidos
derecha; el otro la izquierda. Si observamos detenidamente las ilustraciones de Tenniel, especialmente la que muestra los dos gemelos uno frente a otro, vestidos para la batalla, veremos que los ha dibujado como si fueran enantiomorfos.
para la batalla, veremos que los ha dibujado como si fueran enantiomorfos.

Claro que, algunos son más completos
completos
En el comportamiento y los hábitos de los seres humanos hay muchos ejemplos de marcada asimetría; los más evidentes son consecuencia de que la mayoría de las personas son diestras. La mano derecha está controlada por la parte izquierda del cerebro, y la parte derecha de éste controla la mano izquierda, por lo que la condición de diestro es, en realidad, un fenómeno de lateralidad izquierda del cerebro. Hubo un tiempo en el que se creía que los bebés nacían sin tendencia alguna de tipo genético que favoreciera el uso de una mano concreta, que la lateralidad de un niño era exclusivamente el resultado de las enseñanzas de sus padres. Platón era un notable defensor de esta opinión.

“En el uso de las manos estamos, y estábamos, viciados por las manías de nuestras intitutrices y madres -escribe Platón en sus Leyes-, pues aunque nuestros miembros están compensados por naturaleza, creamos una diferencia entre ellos como consecuencia de un mal hábito.”
Sabemos hoy en día que Platón estaba equivocado. Como hace notar Aristóteles con buen criterio. De todas las maneras, la tendencia innata para muchas personas de usar preferentemente la mano derecha es común desde que la historia puede constatarlo de manera evidente.
puede constatarlo de manera evidente.

Losantropólogs culturales no han encontrado todavía ni una sola sociedad, o incluso una tribu local , en la que la norma sea la lateralidad izquierda: los esquimos, los indios americanos, los maoríes y los africanos son todos diestros. Los antiguos egipcios, griegos y romanos eran diestros. Naturalmente, si retrocemos todavía más en la Historia, la evidencia de la lateralidad diestra es ya escasa e indirecta y hay que dilucidarla a partir del estudio de la forma de sus utensilios y armas, así como de las pinturas que muestran los hombres trabajando o en la batalla.
, en la que la norma sea la lateralidad izquierda: los esquimos, los indios americanos, los maoríes y los africanos son todos diestros. Los antiguos egipcios, griegos y romanos eran diestros. Naturalmente, si retrocemos todavía más en la Historia, la evidencia de la lateralidad diestra es ya escasa e indirecta y hay que dilucidarla a partir del estudio de la forma de sus utensilios y armas, así como de las pinturas que muestran los hombres trabajando o en la batalla.
Las propias palabras que se usan en muchas lenguas para designar la izquierda y la derecha dan testimonio de un sesgo universal hacia el lado derecho. En castellano , ir a derechas es hacer las cosas correctamente, mientras que no dar una a derechas, es sinónimo de hacerlo todo mal.
, ir a derechas es hacer las cosas correctamente, mientras que no dar una a derechas, es sinónimo de hacerlo todo mal.
Ser diestro en algo es lo mismo que poseer una habilidad especial para ello, mientras que una cosa siniestra (del latín sinester, izquierda) es una cosa hecha con mala intención. En otras lenguas el significado viene a ser más o menos el mismo. Los italianos, tan suyos ellos, llaman a la mano izquierda stanca, fatigada, o manca, la que no se tiene. Lo cierto es que, por lo general , los zurdos son ambidiestros.
, los zurdos son ambidiestros.
Para tener una buena visión histórica de mlos prejuicios virulentos contra los zurdos en cualquier parte del mundo, veáse el séptimo capítulo de The Dragons of Eden, de Carl Sagan (Random House, 1977), y el delicioso libro de Jack Fincher, Sinister People (Putnam, 1977). Este último da una lista de más de cien personajes famosos que fueron zurdos.
de Jack Fincher, Sinister People (Putnam, 1977). Este último da una lista de más de cien personajes famosos que fueron zurdos.

Por lo general , y hasta donde sabemos, la especie humana tiene la tendencia a utilizar la mano derecha. Claro que no sabemos. La mayoría de los mamíferos subhumanos son ambidiestros y, ¿cómo serán las especies que viven en otros mundos? El personaje de arriba, al menos, parece que es zurdo.
, y hasta donde sabemos, la especie humana tiene la tendencia a utilizar la mano derecha. Claro que no sabemos. La mayoría de los mamíferos subhumanos son ambidiestros y, ¿cómo serán las especies que viven en otros mundos? El personaje de arriba, al menos, parece que es zurdo.
Lo cierto es que, poco importa si somos zurdos o no, la igualdad en lo esencial es casi idéntica. La verdadera diferencia está en el cerebro, en la manera de ver las cosas, en cómo cada cual enfoca los problemas y qué soluciones aplica a cada situación, en que perspectiva podamos tener de nuestra Sociedad, de nuestras leyes, de nuestros derechos, de la moral y la ética… Todo lo demás, son circunstancias anecdóticas que poco influyen en el devenir del mundo.
Emilio Silvera V.
Abr
19
Las moléculas portadoras de información
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (0)
Comments (0)

En esta Nebulosa molecular gigante, no solo surgen nuevas estrellas y nuevos mundo, también surgen moléculas esenciales para la vida. La Química ahí presente hace de la gigantesca Nebulosa un laboratorio fantástico.
¡La Física! Cuando se asocia a otras disciplinas ha dado siempre un resultado espectacular y, en el caso de la Astronomía, cuando se juntó con la Física, surgió esa otra disciplina que llamamos Astrofísica. La Astrofísica es esa nueva rama de la Astronomía que estudia los procesos físicos y químicos en los que intervienen los fenómenos astronómicos. La Astrofísica se ocupa de la estructura y evolución estelar (incluyendo la generación y transporte de energía en las estrellas), las propiedades del medio interestelar y sus interacciones en sus sistemas estelares y la estructura y dinámica de los sistemas de estrellas (como cúmulos y galaxias) y sistemas de galaxias. Se sigue con la Cosmología que estudia la naturaleza, el origen y la evolución del universo. Existen varias teorías sobre el origen y evolución del universo (big bang, teoría del estado estacionario, etc.
Podríamos decir que, con el párrafo anterior, he descrito perfectamente la esencia de la Astrofísica y la Cosmología! Es fascinante cómo la unión de la física clásica y moderna con la observación astronómica cambió nuestra forma de entender el universo.
Las estrellas, como todo en el Universo, no son inmutables y, con el paso del Tiempo, cambian para convertirse en objetos diferenters de los que, en un principio eran. Por el largo trayecto de sus vidas, transforman los materiales simples en materiales complejos sobre los que se producen procesos biológico-químicos que, en algunos casos, pueden llegar hasta la vida.

No podemos dejar de mirar la inmensidad del Universo, ahí se han formado los materiales de los que estamos hechos los seres vivos, miramos con la esperanza de recibir las respuestas a las preguntas planteadas que nadie ha sabido contestar.
Jefe Indio Seattle (1786 – 1866)
Antiguo es el mundo, pero parece que por fin empezamos a mirar los detalles y a buscar una forma de vida más ecológica, y al fin y al cabo, mejor para nosotros, ya que uno sin lo otro no sería posible. En este articulo hablamos del Jefe indio Seattle, un jefe indio que tuvo que negociar con el progreso que el hombre blanco implantó en las tierras de América, tierras en las que habían convivido en paz durante tantas generaciones y con el respeto hacia unos medios naturales que más tarde fueron explotados sin consideración, todo lo contrario a lo que indicaban las doctrinas de su pueblo.

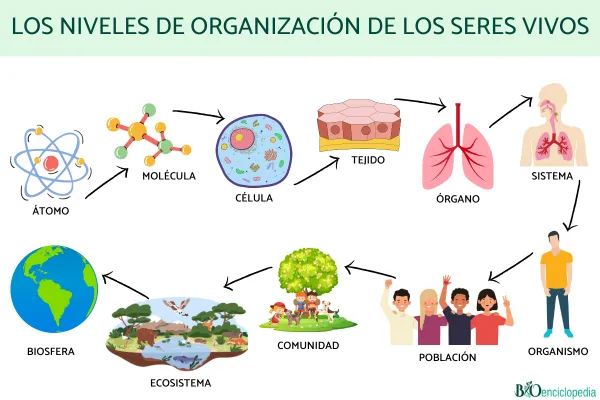
Los organismos vivos somos sistemas extremadamente complejos, formados por un elevado número de elementos interrelacionados que deben mantener sus características a lo largo del tiempo, de una generación a otra. Esto supone que debe existir algún mecanismo para que cada elemento de los organismos se elabore de acuerdo a un “plan”, a un modelo de organización establecido, y que ese modelo pueda ser transmitido de una célula a sus descendientes. Esta necesidad de los seres vivos nos acerca a la noción de información genética.
La información, cualquier tipo de información, es un conjunto organizado de que pueden ser utilizados en algún proceso. En el caso de los seres vivos, los datos se refieren, fundamentalmente, a cómo son las moléculas (en particular las proteínas y el ARN) que la célula necesita producir y a cuándo deben ser elaboradas. La información necesita siempre una memoria, es decir, un sistema físico en el que pueda registrarse, almacenarse y que permita su lectura. En los seres vivos, que somos máquinas químicas, el soporte de la información es un tipo de molécula, concretamente un ácido nucleico. La información que almacenan los organismos recibe el nombre de información genética.

Representación esquemática de la molécula de ADN, la molécula portadora de la información genética. Las moléculas se forman por la Asociación de dos o más átomos, que se mantienen juntas por medio de enlaces químicos. Podríamos decir que algunas moléculasd de vida serían:





– Agua.
– Hidratos de carbono.
– Lípidos.
– Proteínas.
– Acidos Nucleicos.

Principios inmediatos o biomoléculas: cada una de las sustancias que componen la materia viva.
– Simples: O2
– inorgánicos: agua…
– Compuestos:
– orgánicos: glúcidos, lípidos,
proteínas, ac. nucleicos
La enorme variedad de formas, colores, comportamientos, etc que acompaña a los objetos, incluidos los vivientes, sería una consecuencia de la riqueza en la información que soportan las moléculas (y sus agregados) que forman parte de dichos objetos. Ello explicaría que las moléculas de la vida sean en general de grandes dimensiones (macromoléculas). La inmensa mayoría de ellas contiene carbono. Debido a su tetravalencia y a la gran capacidad que posee dicho átomo para unirse consigo mismo, dichas moléculas pueden considerarse como un esqueleto formado por cadenas de esos átomos.

El carbono no es el único átomo con capacidad para formar los citados esqueletos. Próximos al carbono en la tabla periódica, el silicio, fósforo y boro comparten con dicho átomo esa característica, si bien en un grado mucho menor. Refiriéndonos al silicio, señalaremos que las “moléculas” que dicho átomo forma con el oxígeno y otros átomos, generalmente metálicos poseyendo gran nivel de información, difieren en varios aspectos de las moléculas orgánicas, es decir, de las que poseen un esqueleto de átomos de carbono.


El mundo de los silicatos es de una gran diversidad, existiendo centenares de especies minerológicas. Esas diferencias se refieren fundamentalmente a que el enlace químico en el caso de las moléculas orgánicas es covalente, y cuando se forma la sustancia correspondiente (cuatrillones de moléculas) o es un líquido, como es el caso de los aceites, o bien un sólido que funde fácilmente. Entre las moléculas que lo forman se ejercen unas fuerzas, llamadas de Van der Waals, que pueden considerarse como residuales de las fuerzas electromagnéticas, algo más débiles que éstas. En cambio, en los silicatos sólidos (como en el caso del topacio) el enlace covalente o iónico no se limita a una molécula, sino que se extiende en el espacio ocupado por el sólido, resultando un entramado particularmente fuerte.

Al igual que para los cristales de hielo, en la mayoría de los silicatos la información que soportan es pequeña, aunque conviene matizar este punto. Para un cristal ideal así sería en efecto, pero ocurre que en la realidad el cristal ideal es una abstracción, ya que en el cristal real existen aquí y allá los llamados defectos puntuales que trastocan la periodicidad espacial propia de las redes ideales. Precisamente esos defectos puntuales podían proporcionar una mayor información.
El cristal ideal no existe, en su natural, todos tienen inperfecciones y, sólo el elaborado, se podría decir que son cristales perfectos y, sin embargo, la mano del hombre lo que ha producido con tal intervención es perder una valiosa información inserta en ese cuerpo natural.

Si prescindimos de las orgánicas, el resto de las moléculas que resultan de la combinación entre los diferentes átomos no llega a 100.000, frente a los varios millones de las primeras. Resulta ranozable suponer que toda la enorme variedad de moléculas existentes, principalmente en los planetas rocosos, se haya formado por evolución de los átomos, como corresponde a un proceso evolutivo. La molécula poseería mayor orden que los átomos de donde procede, esto es, menor entropía. En su formación, el ambiente se habría desordenado al ganar entropía en una cierta cantidad tal, que arrojarse un balance total positivo.
No puedo dejar pasar la oportunidad, aunque sea de pasada, de mencionar las sustancias.


Las así llamadas, son cuerpos formados por moléculas idénticas, entre las cuales pueden o no existir enlaces químicos. Veremos varios ejemplos. Las sustancias como el oxígeno, cloro, metano, amoníaco, etc, se presentan en estado gaseoso en figuras ordinarias de presión y temperatura. Para su confinamiento se embotellan, aunque existen casos en que se encuentran mezcladas en el aire (os podéis dar una vueltecita por el polo químico de Huelva en España).
En cualquier caso, un gas como los citados consiste en un enjambre de las moléculas correspondientes. Entre ellas no se ejercen fuerzas, salvo cuando colisionan, lo que hacen con una frecuencia que depende de la concentración, es decir, del número de ellas que están concentradas en la unidad de volumen; número que podemos calcular conociendo la presión y temperatura de la masa de gas confinada en un volumen conocido.
Nubes moleculares en Orión
Decía que no existen fuerzas entre las moléculas de un gas. En realidad es más exacto que el valor de esas fuerzas es insignificante porque las fuerzas residuales de las electromagnéticas, a las que antes me referí, disminuyen más rápidamente con la distancia que las fuerzas de Coulomb; y esta distancia es ordinariamente de varios diámetros moleculares.
Podemos conseguir que la intensidad de esas fuerzas aumente tratando de disminuir la distancia media entre las moléculas. Esto se puede lograr haciendo descender la temperatura, aumentando la presión o ambas cosas. Alcanzada una determinada temperatura, las moléculas comienzan a sentir las fuerzas de Van der Waals y aparece el estado líquido; si se sigue enfriando aparece el sólido. El orden crece del gas al líquido, siendo el sólido el más ordenado. Se trata de una red tridimensional en la que los nudos o vértices del entramado están ocupados por moléculas.
Todas las sustancias conocidas pueden presentarse en cualquiera de los tres estados de la materia (estados ordinarios y cotidianos en nuestras vidas del día a día).

El Plasma de las estrellas y otros cuerpos estelares forman el estado más común de la materia en nuestro Universo -al menos la que podemos observar-. El estado de la materia más común que conocemos es el plasma que es la forma que adopta en aquellos estados de altas energías como los que están presentes en las estrellas de las galaxias, los remanentes de supernovas, estrellas de neutrones y otros objetos celestes que adoptan ese estado material que emite una alta radiación.
Si las temperaturas reinantes, son de miles de millones de grados, el estado de la materia es el plasma, el material más común del universo, el de las estrellas (aparte de la materia oscura, que no sabemos ni lo que es, ni donde está, ni que “estado” es el suyo).
En condiciones ordinarias de presión, la temperatura por debajo de la cual existe el líquido y/o sólido depende del tipo de sustancia. Se denomina temperatura de ebullición o fusión la que corresponde a los sucesivos equilibrios (a presión dada) de fases: vapor ↔ líquido ↔ sólido. Estas temperaturas son muy variadas, por ejemplo, para los gases nobles son muy bajas; también para el oxígeno (O2) e hidrógeno (H2). En cambio, la mayoría de las sustancias son sólidos en condiciones ordinarias (grasas, ceras, etc).
Sustancias Compuestas y simples:
Las sustancias pueden ser simples y compuestas, según que la molécula correspondiente tenga átomos iguales o diferentes. El número de las primeras es enormemente inferior al de las segundas.
El concepto de molécula, como individuo físico y químico, pierde su significado en ciertas sustancias que no hemos considerado aún. Entre ellas figuran las llamadas sales, el paradigma de las cuales es la sal de cocina.


Es requerida por el organismo para mantener la volemia y procurar el adecuado equilibrio electrolítico. Además, conserva isotonicidad entre plasma e intersticio, así como también mantiene equilibrio con la célula. Implicada directa en el mantenimiento de la presión arterial media y en el equilibrio osmolar. Su disociación en sangre es parcial (sólo un 93 porciento).
Se trata de cloruro de sodio, por lo que cualquier estudiante de E.G.B. escribiría sin titubear su fórmula: Cl Na. Sin embargo, le podríamos poner en un aprieto si le preguntásemos dónde se puede encontrar aisladamente individuos moleculares que respondan a esa composición. Le podemos orientar diciéndole que en el gas Cl H o en el vapor de agua existen moléculas como individualidades. En realidad y salvo casos especiales, por ejemplo, a temperaturas elevadas, no existen moléculas aisladas de sal, sino una especie de molécula gigante que se extiende por todo el cristal. Este edificio de cristal de sal consiste en una red o entramado, como un tablero de ajedrez de tres dimensiones, en cuyos nudos o vértices se encuentran, alternativamente, las constituyentes, que no son los átomos de Cl y Na sino los iones Cl– y Na+. El primero es un átomo de Cl que ha ganado un electrón, completándose todos los orbitales de valencia; el segundo, un átomo de Na que ha perdido el electrón del orbital s.


Por esta zona de Huelva, conocida como Marismas del Odiel, llevaba con frecuencia a mis hijos pequeños que, jugando por aquellos parajes, se lo pasaban estupendamente, y, de camino, tenía la oportunidad de despertarles la curiosidad de cómo se producía la Sal en el medio natural dejando que se evapore el agua del Mar por los efectos del calor radiado por el Sol que dejaba, finalmente, la Sal al descubierto para ser refinada y vendida comercialmente.
Cuando los átomos de Cl y Na interaccionan por aproximarse suficientemente sus nubes electrónicas, existe un reajuste de cargas, porque el núcleo de Cl atrae con más fuerza los electrones que el de Na, así uno pierde un electrón que gana el otro. El resultado es que la colectividad de átomos se transforma en colectividad de iones, positivos los de Na y negativos los de Cl. Las fuerzas electromagnéticas entre esos iones determinan su ordenación en un cristal, el Cl Na. Por consiguiente, en los nudos de la red existen, de manera alternativa, iones de Na e iones de Cl, resultando una red mucho más fuerte que en el caso de que las fuerzas actuantes fueran de Van der Waals. Por ello, las sales poseen puntos de fusión elevados en relación con los de las redes moleculares.
Emilio Silvera V.
Feb
24
Las colisiones galácticas resultan en estallidos de formación estelar
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (0)
Comments (0)

Esta imagen es una instantánea de la simulación de la colisión entre las dos galaxias Antennae ((NGC 4038 y NGC 4039)). Las estrellas se forman en las regiones más densas (amarillo y rojo) debido a los efectos de compresión turbulenta.
Crédito: F. Renaud/CEA – Sap.
Mediante el uso de simulaciones sofisticadas, los científicos creen que finalmente han resuelto uno de los misterios que llevaba años atormentando a los astrónomos:


Estas colisiones producen gran nacimiento de estrellas nuevas
¿Por qué las colisiones entre galaxias desencadenan olas o ráfagas de formación estelar?
Las estrellas se forman dentro de una nube de gas y polvo, cuando ésta se torna lo suficientemente densa como para colapsar, normalmente bajo el efecto de la gravedad. Sin embargo, cuando las galaxias chocan, o se unen, se produce un aumento del flujo del gas hacia el centro de la galaxia, lo que hace que el gas se mueva de una manera muy aleatoria.
Este aumento en la turbulencia debería, en teoría, frenar o incluso cesar por completo el colapso de la nube, y evitar así la formación de estrellas, pero en realidad ocurre todo lo contrario.
Con el fin de averiguar por qué está ocurriendo esto, un equipo de astrofísicos franceses, liderado por Florent Renaud, se dirigió a los superordenadores más potentes de Europa para modelar dos sistemas diferentes.
El primero, que requirió 12 millones de horas de tiempo de cálculo, tenía como objetivo modelar una galaxia similar a la Vía Láctea y simular las condiciones del ambiente alrededor de esta galaxia (con un diámetro de 300.000 años luz). Luego, el equipo modeló dos galaxias colisionando a través de 600.000 años luz, lo que requirió 8 millones de horas de computación. La alta resolución de estos modelos otorgó a los científicos con un gran nivel de detalle, lo que dio lugar a algunos resultados interesantes.
Los modelos demostraron que cuando dos galaxias colisionan, en lugar de ir girando, el gas entra en un estado de compresión. Esto genera un exceso de gas denso que se colapsa por efecto de la gravedad, y da lugar a la formación de estrellas. Decimos que ambas galaxias experimentan un brote estelar.
Florent dijo: “Este es un gran paso hacia adelante en nuestra comprensión de la formación estelar, algo que sólo se hizo posible gracias al avance en paralelo de la potencia de las computadoras. Estos sistemas ayudan a entender mejor y con más detalle la naturaleza de las galaxias y de sus contenidos”.
Fuente: Cosmo Noticias.
Nov
26
La necesidad agudiza la imaginación
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (0)
Comments (0)
La fuerza nuclear débil nos habla de materiales que, de manera natural, emiten radiación y se desintegran. Al pensar en la desintegración me ha traído a la memoria aquellos libros de Asimov que nos explicaba cuestiones de ciencia y nos decía existen materiales que también se desintegran de manera natural y que son materiales fértiles, o que sin serlo, se pueden transformar en otros que sí lo son.
se desintegran de manera natural y que son materiales fértiles, o que sin serlo, se pueden transformar en otros que sí lo son.
Al hablar de material fértil me estoy refiriendo a núclidos que pueden absorber neutrones para formar material fisible. El uranio-238, por ejemplo, absorbe un neutrón para formar uranio-239, que se desintegra en plutonio-239. Este es el tipo
formar material fisible. El uranio-238, por ejemplo, absorbe un neutrón para formar uranio-239, que se desintegra en plutonio-239. Este es el tipo de conversión que la imaginación del hombre hace que ocurra en un reactor reproductor.
de conversión que la imaginación del hombre hace que ocurra en un reactor reproductor.

Lo explicaré con más detalles: El Reactor Reproductor Rápido es un reactor de neutrones rápidos diseñado para producir combustible generando más material fisible del que consume. El FBR es uno de los tipos posibles de reactores reproductores.
producir combustible generando más material fisible del que consume. El FBR es uno de los tipos posibles de reactores reproductores.


Veamos: El uranio-235 es un combustible práctico, es decir, los neutrones lentos son capaces de hacer que el uranio-235 se fisione, o lo que es lo mismo, se rompan sus átomos en dos, produciendo neutrones lentos, que a su vez inducen otras fisiones atómicas. El uranio-233 y el plutonio-239 son también combustibles nucleares prácticos por las mismas razones.
que el uranio-235 se fisione, o lo que es lo mismo, se rompan sus átomos en dos, produciendo neutrones lentos, que a su vez inducen otras fisiones atómicas. El uranio-233 y el plutonio-239 son también combustibles nucleares prácticos por las mismas razones.
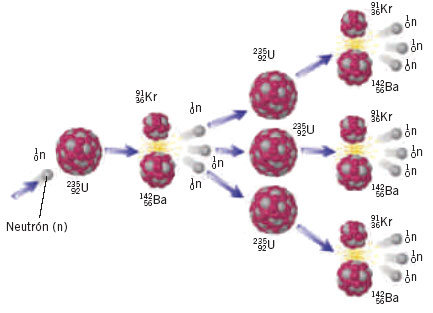
Desgraciadamente, el uranio-233 y el plutonio-239 no existen en estado natural sino en trazas mínimas, y el uranio-235, aunque existe en cantidades apreciables, no deja de ser raro. En cualquier muestra de uranio natural, sólo siete de cada mil átomos son de uranio-235, el resto es uranio-238.
natural sino en trazas mínimas, y el uranio-235, aunque existe en cantidades apreciables, no deja de ser raro. En cualquier muestra de uranio natural, sólo siete de cada mil átomos son de uranio-235, el resto es uranio-238.

Uranio
El uranio natural extraído de las minas contiene un 99´3 % de U-238 y apenas el 0´7 % de U-235.
El uranio-238, la variedad común de uranio, no es un combustible nuclear práctico. Así que, el uranio que más abunda en la naturaleza no sirve como combustible nuclear. Podemos conseguir que se fisione, pero sólo con neutrones rápidos. Los átomos de uranio-238 que se rompen en dos, producen neutrones lentos, que no bastan para producir o inducir nuevas fisiones. El uranio-238 cabría compararlo a la madera húmeda: es posible hacer
combustible nuclear. Podemos conseguir que se fisione, pero sólo con neutrones rápidos. Los átomos de uranio-238 que se rompen en dos, producen neutrones lentos, que no bastan para producir o inducir nuevas fisiones. El uranio-238 cabría compararlo a la madera húmeda: es posible hacer que arda, pero acabará por apagarse.
que arda, pero acabará por apagarse.

El uranio es un elemento químico metálico de color plateado-grisáceo de la serie de los actínidos, su símbolo químico es U y su número atómico es 92. Por ello posee 92 protones y 92 electrones, con una valencia de 6. Su núcleo puede contener entre 142 y 146 neutrones, sus isótopos más abundantes son el 238U que posee 146 neutrones y el 235U con 143 neutrones. El uranio tiene el mayor peso atómico de entre todos los elementos que se encuentran en la naturaleza. El uranio es aproximadamente un 70% más denso que el plomo, aunque menos denso que el oro o el wolframio. Es levemente radioactivo. Fue descubierto como óxido en 1789 por M. H. Klaproth que lo llamó así en el honor del planeta Urano que acababa de ser descubierto en 1781.
Supongamos, sin embargo, que se separa el uranio-235 del uranio-238 (trabajo más bien difícil) y que se utiliza aquel para hacer funcionar un reactor nuclear. Los átomos de uranio-235 que forman el combustible del reactor se fisionan y esparcen miríadas de neutrones lentos en todas direcciones. Si el reactor está rodeado por una capa de uranio ordinario (que en su mayor parte
más bien difícil) y que se utiliza aquel para hacer funcionar un reactor nuclear. Los átomos de uranio-235 que forman el combustible del reactor se fisionan y esparcen miríadas de neutrones lentos en todas direcciones. Si el reactor está rodeado por una capa de uranio ordinario (que en su mayor parte es uranio-238), los neutrones que van a parar allí son absorbidos por el uranio-238 y, aunque no pueden hacer que el uranio-238 se fisione, sí pueden provocar otros cambios que finalmente, producirán plutonio-239. Separando este plutonio-239 del uranio (tarea muy fácil), puede ser utilizado como combustible nuclear practico para la fisión.
es uranio-238), los neutrones que van a parar allí son absorbidos por el uranio-238 y, aunque no pueden hacer que el uranio-238 se fisione, sí pueden provocar otros cambios que finalmente, producirán plutonio-239. Separando este plutonio-239 del uranio (tarea muy fácil), puede ser utilizado como combustible nuclear practico para la fisión.
De esta manera, el reactor nuclear genera nuevo combustible a partir de un material (uranio-238) que no lo es. Este es el motivo de que al reactor nuclear que hace posible la transformación se le llame “reactor generador”.
combustible a partir de un material (uranio-238) que no lo es. Este es el motivo de que al reactor nuclear que hace posible la transformación se le llame “reactor generador”.
Un reactor generador bien diseñado puede producir más plutonio-239 que el uranio-234 consumido para ello. De este modo, las reservas totales de uranio de la Tierra (y no sólo las de uranio-235) se convierten en potenciales de combustible nuclear.
Torio
Carlo Rubbia, exdirector del CERN (los mismos que hicieron el Colisionador de Hadrones) y ganador del premio Nobel de física en 1984, ha trabajado buena parte de su carrera en el desarrollo de tecnologías para la producción de energía a partir de torio y calcula que con un reactor adecuado, este proceso de fisión podría generar a partir de 1 tonelada del elemento la misma cantidad de energía que 200 toneladas de uranio y 3.500.000 toneladas de carbón.
de su carrera en el desarrollo de tecnologías para la producción de energía a partir de torio y calcula que con un reactor adecuado, este proceso de fisión podría generar a partir de 1 tonelada del elemento la misma cantidad de energía que 200 toneladas de uranio y 3.500.000 toneladas de carbón.
El torio, tal como se da en la naturaleza, consiste todo él en torio-232, que al igual que el uranio-238, no es un combustible nuclear práctico, porque requiere neutrones rápidos para fisionarse. Pero si se coloca torio-232 alrededor de un reactor nuclear, sus átomos absorberán los neutrones y, sin experimentar fisión alguna, se convertirán en átomos de uranio-233. Como
se da en la naturaleza, consiste todo él en torio-232, que al igual que el uranio-238, no es un combustible nuclear práctico, porque requiere neutrones rápidos para fisionarse. Pero si se coloca torio-232 alrededor de un reactor nuclear, sus átomos absorberán los neutrones y, sin experimentar fisión alguna, se convertirán en átomos de uranio-233. Como el uranio-233 es un combustible práctico que se puede separar fácilmente del torio, el resultado es otra variedad del reactor generador, que convierte las reservas de torio en un combustible nuclear en potencia.
el uranio-233 es un combustible práctico que se puede separar fácilmente del torio, el resultado es otra variedad del reactor generador, que convierte las reservas de torio en un combustible nuclear en potencia.


Hasta que no se descubra otra manera de producir energía, el Uranio seguirá
que no se descubra otra manera de producir energía, el Uranio seguirá
La cantidad total de uranio y de torio que hay en la Tierra es unas 800 veces mayor que las reservas de uranio-235, lo que significa que el buen uso de los reactores generadores podría multiplicar por 800 la oferta potencial de energía extraída de plantas de fisión nuclear.
En este punto, sin dejar de elogiar la inteligencia del hombre que ha sabido encontrar la manera de transformar una materia inservible en otra practica, hay que decir que la energía de fisión nuclear genera también muchos problemas.
Como estará comprobando al lector de este trabajo , el autor ha querido esta vez diversificar los temas y plasmar una variedad múltiple que facilite el conocimiento de distintas cosas que ocurren en la naturaleza, o que la mano del hombre hace que ocurran, y todas estas cuestiones tratadas aquí van encaminadas a resolver preguntas que en alguna ocasión nos hemos podido hacer
, el autor ha querido esta vez diversificar los temas y plasmar una variedad múltiple que facilite el conocimiento de distintas cosas que ocurren en la naturaleza, o que la mano del hombre hace que ocurran, y todas estas cuestiones tratadas aquí van encaminadas a resolver preguntas que en alguna ocasión nos hemos podido hacer , tales como:
, tales como:
¿Por qué al calentar un metal se pone primero rojo, luego naranja, después amarillo, pero a continuación blanco en lugar de seguir el espectro y ponerse verde?
¿Y el color en las estrellas?


Cuando un herrero está trabajando, el metal adquiere diferentes colores según recibe el calor de la fragua. Primero se mostrará de un rojo intenso, para ir progresivamente adoptando tonos más claros, pasando del anaranjado al amarillo, y por fin al blanco.
ir progresivamente adoptando tonos más claros, pasando del anaranjado al amarillo, y por fin al blanco.
Si se pudiera seguir calentando el hierro, éste adquiriría tonos azulados. Estos cambios en la coloración son una consecuencia directa del aumento de la temperatura, que permitirá mayor maleabilidad. El Cúmulo del Joyero (en la constelación de la Cruz del Sur), fotografiado arriba, muestra cómo ocurre lo mismo con las estrellas, de manera que encontraremos estrellas azules, las más calientes, blancas, amarillas, anaranjadas y rojas, las más “frías”. A veces, estos colores pueden percibirse a simple vista, como Antares (Alpha Scorpii) que es de color rojo, o Rigel (Beta Orionis) blanco-azulada.
Antares (Alpha Scorpii) que es de color rojo, o Rigel (Beta Orionis) blanco-azulada.
En la Naturaleza rigen las mismas leyes para todos y, en todas partes se producen los mismos fenómenos debidos a las mismas causas, en este caso: ¡La Temperatura!
todos y, en todas partes se producen los mismos fenómenos debidos a las mismas causas, en este caso: ¡La Temperatura!
Cualquier objeto, a cualquier energía superior al cero absoluto, radia ondas electromagnéticas. Si su temperatura es muy baja, emite sólo ondas de radio largas, muy pobres en energías. Al aumentar la temperatura, radia una cantidad mayor de ondas, pero también empieza a radiar ondas de radio más cortas (y más energéticas). Si la temperatura sigue subiendo, empiezan a radiarse microondas aún más energéticas y después radiaciones infrarrojas.
empieza a radiar ondas de radio más cortas (y más energéticas). Si la temperatura sigue subiendo, empiezan a radiarse microondas aún más energéticas y después radiaciones infrarrojas.


Esto no quiere decir que a una temperatura dada sólo se emitan ondas de radio largas, un poco más arriba sólo ondas de radio cortas, luego sólo microondas y después sólo infrarrojos. En realidad, se emite toda la gama de radiaciones, pero siempre hay una radiación máxima, es decir, una gama de longitudes de onda que son las más radiadas, flanqueadas por cantidades menores en el lado de las energías bajas y por cantidades todavía más pequeñas en el de las altas.
Cuando un objeto alcanza la temperatura del cuerpo humano (37°C), el máximo de radiación se encuentra en los infrarrojos largos. El cuerpo humano también radia ondas de radio, pero las longitudes de ondas más cortas y más energéticas son siempre las más fáciles de detectar por ser los más potentes.
un objeto alcanza la temperatura del cuerpo humano (37°C), el máximo de radiación se encuentra en los infrarrojos largos. El cuerpo humano también radia ondas de radio, pero las longitudes de ondas más cortas y más energéticas son siempre las más fáciles de detectar por ser los más potentes.
Cuando la temperatura alcanza aproximadamente los 600°C, el máximo de radiación se halla en el infrarrojo corto. Pero a estas alturas la pequeña cantidad de radiación que se halla en el lado de las energías altas adquiere una importancia especial, porque entra ya en la región de la luz visible roja. El objeto reluce entonces con un rojo intenso.
Este rojo constituye sólo un pequeño porcentaje de la radiación total, pero como da la casualidad de que nuestro ojo lo percibe, le otorgamos toda nuestra atención y decimos que el objeto está al “rojo vivo”.
da la casualidad de que nuestro ojo lo percibe, le otorgamos toda nuestra atención y decimos que el objeto está al “rojo vivo”.
Si la temperatura sigue subiendo, el máximo de radiación continúa desplazándose hacia las longitudes de ondas cortas y cada vez se emite más luz visible de longitudes cada vez menores. Aunque el objeto radia más luz roja, se van agregando poco a poco luz anaranjada y luz amarilla en cantidades menores pero significativas. Al llegar a los 1.000°C la mezcla de colores la percibimos como naranja, y a los 2.000°C como amarilla. Lo cual no significa que a los 1.000°C sólo se radie luz naranja y a los 2.000°C sólo se radie luz amarilla, porque si fuese así, habría efectivamente que esperar que lo siguiente fuese “color verde”. Lo que en realidad vemos son mezclas de colores.
las longitudes de ondas cortas y cada vez se emite más luz visible de longitudes cada vez menores. Aunque el objeto radia más luz roja, se van agregando poco a poco luz anaranjada y luz amarilla en cantidades menores pero significativas. Al llegar a los 1.000°C la mezcla de colores la percibimos como naranja, y a los 2.000°C como amarilla. Lo cual no significa que a los 1.000°C sólo se radie luz naranja y a los 2.000°C sólo se radie luz amarilla, porque si fuese así, habría efectivamente que esperar que lo siguiente fuese “color verde”. Lo que en realidad vemos son mezclas de colores.
Al llegar a los 6.000°C (la temperatura superficial del Sol), el máximo de radiación está en el amarillo visible y lo que llega a nuestros ojos son grandes cantidades de luz visible, desde el violeta hasta el rojo. La incidencia simultánea de toda la gama de luz visible sobre nuestra retina nos da la sensación de blanco, y de ahí el color del Sol.
el violeta hasta el rojo. La incidencia simultánea de toda la gama de luz visible sobre nuestra retina nos da la sensación de blanco, y de ahí el color del Sol.
Los objetos más calientes aún que el Sol radian todas las longitudes de ondas de luz visible y en cantidades todavía mayores, pero el máximo de radiación se desplaza al azul, de modo que la mezcla se desequilibra y el blanco adquiere un tinte azulado.
el máximo de radiación se desplaza al azul, de modo que la mezcla se desequilibra y el blanco adquiere un tinte azulado.
Toda esta travesía se produce para objetos calientes que emiten “espectros continuos”, es decir, que radian luz en la forma de una ancha banda de longitudes de ondas. Ciertas sustancias en condiciones adecuadas, radian sólo luz de determinadas longitudes de onda. El nitrato de bario radia luz verde cuando se calienta, y con ese fin se lo utiliza en los fuegos de artificio, “calor verde”, podríamos decir.
adecuadas, radian sólo luz de determinadas longitudes de onda. El nitrato de bario radia luz verde cuando se calienta, y con ese fin se lo utiliza en los fuegos de artificio, “calor verde”, podríamos decir.


Nitrato de Bario que produce el color verde en los bonitos fuegos artificiales
¡Qué bonito es saber! Ya me gustaría.

En alguna ocasión todos hemos oído mencionar la palabra “gases nobles”, y sin embargo no siempre sabemos lo que son y el por qué le llaman así. Los elementos que reaccionan difícilmente o que no reaccionan en absoluto con otros elementos se denominan “inertes”. El nitrógeno y el platino son ejemplos de elementos inertes.
En la última década del siglo pasado se descubrieron en la atmósfera una serie de gases que no parecían intervenir en ninguna reacción química. Estos nuevos gases (helio, neón, argón, kriptón, xenón y radón) son más inertes que cualquier otro elemento y se agrupan bajo el nombre de gases inertes.
de gases inertes.
Los elementos inertes reciben a veces el calificativo de “nobles” porque esa resistencia a reaccionar con otros elementos recordaba un poco a la altanería de la aristocracia. El oro y el platino son ejemplos de “metales nobles”, y por la misma razón se llaman a veces “gases nobles” a los gases inertes. Hasta 1.962, el nombre más común era el de gases inertes, quizá porque lo de nobles parecía poco apropiados en sociedades democráticas.
más común era el de gases inertes, quizá porque lo de nobles parecía poco apropiados en sociedades democráticas.

La complicada historia del flúor
“Los primeros intentos de aislar este elemento dejaron tras de sí una estela de químicos muertos, los llamados “mártires del flúor”.”
El nombre actual del flúor proviene del latín, fluo, que significa fluir. Con esta palabra bautizaron en la edad media al “flúor espato”, un mineral que se utilizaba en las fundiciones para que el hierro se fundiera a menor temperatura y que también reduce la viscosidad del metal líquido, lo que lo ayuda a fluir con más facilidad a través de los canales y moldes. Como el flúor se aisló por primera vez a partir de este aditivo metalúrgico, a la que hoy en día nos referimos más a menudo como fluorita, se decidió dejarle como nombre la palabra latina del mineral.
Debido a su alta reactividad, no conviene estar alrededor del flúor sin unas medidas de protección muy estrictas. De hecho, los primeros intentos de aislar este elemento dejaron tras de sí una estela de químicos muertos, los llamados “mártires del flúor”.
Flúor
El criptón del manto de la Tierra, recolectado de puntos calientes geológicos en Islandia y las Islas Galápagos, revela una imagen más clara de cómo se formó nuestro planeta.
Es apropiado incluir una descripción de este grupo de elementos conocido en un capítulo dedicado a los halógenos, porque el flúor es el único elemento conocido que entra en combinación química directa con los dos gases nobles más pesados, el xenón y el criptón, resultando en compuestos estables.
Los gases nobles surgen en la naturaleza como constituyentes menos abundantes de la atmósfera. La primera indicación de la existencia de los gases nobles fue divulgada por el químico ingles Cavendish, en 1784.
La razón de que los gases inertes sean inertes es que el conjunto de electrones de cada uno de sus átomos está distribuido en capas especialmente estables. La más exterior, en concreto, tiene 8 electrones. Así la distribución electrónica del neón es (2,8) y la del argón (2,8,8). Como la adición o sustracción de electrones rompe esta distribución estable, no pueden producirse cambios electrónicos. Lo cual significa que no pueden producirse reacciones químicas y que estos elementos son inertes.
distribución estable, no pueden producirse cambios electrónicos. Lo cual significa que no pueden producirse reacciones químicas y que estos elementos son inertes.
Ahora bien, el grado de inercia depende de la fuerza con que el núcleo, cargado positivamente y situado en el centro del átomo sujeta a los 8 electrones de la capa exterior. Cuantas más capas electrónicas haya entre la exterior y el centro, más débil será la atracción del núcleo central sobre los electrones de esa última capa de electrones.
bien, el grado de inercia depende de la fuerza con que el núcleo, cargado positivamente y situado en el centro del átomo sujeta a los 8 electrones de la capa exterior. Cuantas más capas electrónicas haya entre la exterior y el centro, más débil será la atracción del núcleo central sobre los electrones de esa última capa de electrones.

El Radón es un gas radiactivo de origen natural procedente de la desintegración radiactiva de pequeñas cantidades de uranio presentes en rocas y suelo, es el responsable de miles de muertes por cáncer de pulmón en Europa cada año. El gas se filtra en los edificios a través del suelo y de los sótanos, puede acumularse llegando a niveles elevados, especialmente en espacios cerrados y poco ventilados.
Quiere esto decir que el gas inerte más complejo es también el menos inerte. El gas inerte de estructura atómica más complicada es el radón. Sus átomos tienen una distribución electrónica de (2,8,18,32,18,8). El radón, sin embargo está sólo constituido por isótopos radiactivos y es un elemento con el que difícilmente se pueden hacer experimentos químicos. El siguiente en orden de complejidad es el xenón, que es estable. Sus átomos tienen una distribución electrónica de (2,8,18,18,8).
experimentos químicos. El siguiente en orden de complejidad es el xenón, que es estable. Sus átomos tienen una distribución electrónica de (2,8,18,18,8).
Se sabe desde hace décadas que la abundancia en la Tierra del xenón es menor de lo que debería ser según las proporciones observadas del resto de gases nobles. Las abundancias de estos gases se usan por los geoquímicos para evaluar y datar los principales procesos terrestres, incluyendo la formación de la atmósfera. Para poder hacerlo parten de una hipótesis básica: que los gases nobles son inertes en toda circunstancia. Un trabajo realizado por Gary Schrobilgen y David Brock, de la Universidad McMaster (Canadá), cuyos resultados se publican en el Journal of the American Chemical Society explica la baja abundancia del xenón y pone en evidencia que el xenón no es tan noble como
realizado por Gary Schrobilgen y David Brock, de la Universidad McMaster (Canadá), cuyos resultados se publican en el Journal of the American Chemical Society explica la baja abundancia del xenón y pone en evidencia que el xenón no es tan noble como se suponía.
se suponía.
Los electrones más exteriores de los átomos de xenón y radón están bastante alejados del núcleo y, por consiguiente, muy sueltos. En presencia de átomos que tienen una gran apetencia de electrones, son cedidos rápidamente. El átomo con mayor apetencia de electrones es el flúor, y así fue como en 1.962 el químico canadiense Neil Bartlett consiguió formar compuestos de xenón y flúor.
Desde entonces se han conseguido formar también compuestos de radón y kriptón. Por eso los químicos rehúyen el nombre de gases inertes, porque a fin de cuentas, esos gases no son completamente inertes. Hoy día se ha impuesto la denominación de “gases nobles”, y existe toda una rama de la química que se ocupa de los “compuestos de gases nobles”.
de gases inertes, porque a fin de cuentas, esos gases no son completamente inertes. Hoy día se ha impuesto la denominación de “gases nobles”, y existe toda una rama de la química que se ocupa de los “compuestos de gases nobles”.

Naturalmente, cuanto más pequeño es el átomo de un gas noble, más inerte es, y no se ha encontrado nada que sea capaz de arrancarles algún electrón. El argón, cuya distribución electrónica es de 2,8,8 y el neón, con 2,8 electrones respectivamente, sigue siendo completamente inerte. Y el más inerte de todos es el helio, cuyos átomos contienen una sola capa electrónica con dos electrones (que es lo máximo que puede alojar esta primera capa) que al estar en la primera linea cerca del núcleo positivo, están fuertemente atraídos al tener su carga eléctrica el signo negativo.
alojar esta primera capa) que al estar en la primera linea cerca del núcleo positivo, están fuertemente atraídos al tener su carga eléctrica el signo negativo.
Para finalizar diré que los gases nobles (gases inertes, gases raros) están clasificados en el grupo 18 (antiguamente 0) de la Tabla periódica de los elementos y se definen por símbolos que responden a: helio (He), neón (Ne), argón (Ar), kriptón (Kr), xenón (Xe) y radón (Rn).
finalizar diré que los gases nobles (gases inertes, gases raros) están clasificados en el grupo 18 (antiguamente 0) de la Tabla periódica de los elementos y se definen por símbolos que responden a: helio (He), neón (Ne), argón (Ar), kriptón (Kr), xenón (Xe) y radón (Rn).

Ya se dijo antes la configuración electrónica de cada uno de ellos y todas las capas internas están completamente ocupadas, lo que hace que estos elementos, por tanto, constituyan la terminación de un periodo y posean configuración de capa completa, por lo que sus energías de ionización son muy elevadas y su reactividad química escasa.
Como son monoatómicos, las moléculas de los gases nobles poseen simetría esférica, y las fuerzas intermoleculares son muy débiles, por lo que sus entalpías de vaporización son muy bajas.
Con todo lo anteriormente expuesto sobre los gases nobles, espero que el lector del trabajo aquí reflejado pueda tener una idea más amplia y un conocimiento más certero sobre lo que en realidad son los denominados como “gases nobles”.
aquí reflejado pueda tener una idea más amplia y un conocimiento más certero sobre lo que en realidad son los denominados como “gases nobles”.
En comparación con la inmensidad del universo, nos queda aún muchísimo que aprender. Si nos limitamos a nuestro entorno más cercano, la Tierra, ¿Cómo hemos podido llegar tan lejos?

Remamos hacia el Horizonte que nunca podremos alcanzar
¡La curiosidad! y ¡La necesidad! ¡El Instinto! y ¡La Evolución! Todo ello, amigos míos, nos lleva a querer saber y, para ello, debemos desvelar los secretos de la Naturaleza, que por cierto, no resulta nada fácil. Llevamos miles de años intentando comprender y, de momento, sólo sabemos… ¡Algunas cosas!
Emilio Silvera V.
Fuente: Variada y destacando, Cien preguntas básicas sobre ciencia de Asimov.
Mar
4
¡La Curiosidad! La madre del saber
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Cosas curiosas ~
Clasificado en Cosas curiosas ~
 Comments (9)
Comments (9)

¡Qué bonito sería si las piedras pudieran hablar! ¿Qué nos contarían éstas?
Todos los asiduos a este lugar, sabéis de mi curiosidad insaciable por las cosas, por lo que pasó, por las Civilizaciones antiguas, por los misterios que la materia encierra, y, en fin, por el Universo y las historias de las criaturas que lo pueblan y que, en la antigüedad, estuvieron aquí.

Ellos inventaron el Cero que cambio po completo las matemáticas, a la izquierda no vale nada pero… ¡A la Derecha…!
En el siglo V, Aryabhata escribe el Aryabhatiya, un delgado volumen concebido para complementar las reglas de cálculo utilizadas en astronomía y en medida matemática. Escrito en verso, carece de rigor lógico o metodología deductiva. Aunque casi la mitad de las entradas son incorrectas, es en el Aryabhatiya en donde el sistema decimal posicional aparece por vez primera. Siglos más tarde, el matemático árabe Abu Rayhan Biruni describiría este tratado como «una mezcla de guijarros ordinarios y cristales onerosos». En 499, Aryabhata.

Existen lugares en los que, se han conservado más vivos y realistas los recuerdos del pasado y, en la India, donde al contrario que en la China, no cruzan el cielo los Dragones, serpientes o Aves monstruosas, nos dicen que fueron máquinas, las que, para el asombro de todos, cruzaban el cielo.

James Churchward, el desconcertante estudioso inglés cuyas investigaciones no son nada desdeñables, siempre y cuando no se aproximan a las especulaciones teo-sofistas, nos habla de un manuscrito que contiene la descripción de una nave aérea de hace 20.000 años.
“La energía” –detalla en una obra redactada varios lustros antes de que se hablara de astronaves y satélites artificiales- se obtiene de la atmósfera de manera simple y poco costosa. En la obra daba una amplia explicación del motor y sus compartimentos y cámaras y de las increíbles propiedades que la nave tenía que, incluso, podía quedar estática en el aire, o, salir disparada como un rayo hacia lo más alto del cielo hasta desaparecer de la vista.

Enormes máquinas voladoras que surcaban los cielos
¿Fantasías? Escuchemos un relato de la Academia Internacional de Investigaciones sánscritas de Mysore: “Los manuscritos cuya traducción del sánscrito presentamos, describen varios tipos de “vimana” (naves que se mueven por sí mismas), capaces de viajar por su propio impulso por tierra, agua y aire, y, asimismo, de planeta a planeta. Parece que los vehículos aéreos podían detenerse en el cielo hasta quedar inmóviles, y que estaban dotados de instrumentos capaces de señalar, incluso a distancia, la presencia de aparatos enemigos.
(El relato fue publicado en la India por el especialista Maharshi Bharadaja con el título Aeronáutica del pasado prehistórico.)
Numerosísimos testimonios nos vienen a confirman ampliamente lo anterior. Por ejemplo tenemos una amplia muestra en el Samaranganasutradhara que narra la historia de vuelos fantásticos realizados por el mundo, y hacia el Sol y las estrellas. Un documento de época precristiana nos suministra una detallada descripción del carro celeste de Rama. La narración nos dice: “…el carro se movía por sí solo y era grande y estaba bien pintado; tenía dos pisos, muchas habitaciones y ventanas…”, cuyas hazañas, canta Valmiki el Herodoto indio: “El carro celeste, que posee una fuerza admirable, alada de velocidad, dorado en su forma y en su esplendor… El carro celeste ascendió por encima de la colina y del valle boscoso…alado como el rayo, dardo de Indra, fatal como el relámpago del cielo, envuelto en humo y destellos flameantes, rápida proa circular” (del Ramayana, que narra la epopeya de Rama).
Centenares y centenares de historias semejantes nos podemos encontrar a lo largo de las tradiciones hundúes: “ahí va la divina Maya volando en un carro de oro circular, que mide 12.000 codos de circunferencia, capaz de alcanzar las estrellas”, y, hete aquí el “caballo metálico del cielo” del rey Satrugit y el “carruaje del aire” del rey Pururavas. También el siglo IV de nuestra era encontramos a un héroe aeronauta, el monje budista Gunarvarman, quien se va desde Ceylán a Java en un aparato similar a los antiguos, sacado quién sabe de dónde.
Según se deduce de estos antiquísimos manuscritos en sánscrito, aquellos hindúes prehistóricos (o lo que realmente pudieran ser), no utilizaban aquellos ingenios voladores para excursiones de placer, sino que, según nos cuentan los relatos, las acciones bélicas eran también cotidianas que describen terribles batallas.
Un bajorrelieve en Angkor Wat (Camboya) representa a Rávana Rávana peleando en la batalla de Lanka, el clímax del Ramaiana.
Rávana, el rey de los demonios de Ceylán, enemigo mortal de Rama, “voló sobre los adversarios (según nos narra un manuscrito del año 500 a, de C.) haciendo caer ingenios que causaron grandes destrucciones. Finalmente, fue capturado y muerto, y su máquina celeste cayó en manos del capitán hindú Ram Chandra, quién, sirviéndose de ella, voló a la capital, Adjhudia…”
Y esto no son más que bagatelas. “El Bhisma Parva –recuerda Drake- menciona armas como la “verga de Brahma” y el “Rayo de Indra”, cuyos efectos se parecen a los producidos por la energía nuclear. El Drona Parva nos habla del “señor Mahadeva” y de sus terribles lanzas volantes (¿misiles?) capaces de destruir ciudades enteras fortificadas…, y describe las fantásticas armas de Agni, que aniquilaron ejércitos completos y devastaron la Tierra como bombas de Hidrógeno.”
¿Es posible que no se hayan conservado trazas de estos alucinantes conflictos? Los restos existen, y numerosísimos –responden los investigadores-. Basta que nos tomemos la molestia de ir en su busca. No es una empresa fácil, desde luego, puesto que, desde hace milenios la jungla se ha espesado sobre las ruinas, pero si consiguiéramos localizar todas las “ciudades muertas” de la gran península, constelaríamos el mapa de la India de tantos puntos como los que, en un Atlas, nos indican los centros de población actuales.

De vez en cuando aparecen descripciones a este respecto que nos dejan perplejos. El explorador De Camp, por ejemplo, refirió haber visto, en la zona que se extiende entre el Ganges y los montes Rajmahal, ruinas carbonizadas por algo que no podía ser un simple incendio, por violento que éste fuera. Algunas piedras gigantescas aparecían fundidas y desenterradas en varios puntos, “como bloques de estaño afectados por la salpicadura de una colada de acero”.
Más al Sur, el oficial británico J. Campbell se topó, en los años veinte, con ruinas similares, y quedó sorprendido por un extrañísimo detalle: en el pavimento semivitrificado de lo que debió de ser un patio interior, parecían haber sido impresas, por una fuerza desconocida, formas de cuerpos humanos.

Otros viajeros refieren haber descubierto en el corazón de los bosques indios ruinas de edificios nunca vistos, con paredes “semejantes a gruesas losas de cristal” asimismo perforadas, resquebrajadas y corroídas por agentes desconocidos. Y habiendo penetrado en una de estas construcciones, parecida a una cúpula baja, el explorador y cazador H. J. Hamilton se encontró con la mayor sorpresa de su vida.ç
“En una parte –recuerda-, el suelo cedió bajo mis pies con un extraño crujido. Me puse a seguro y, luego, ensanché con la culata del fusil el boquete que se había abierto, y me introduje en él. Me encontré en una estancia larga y estrecha que recibía luz por una grieta de la bóveda. Al fondo, vi una especie de mesa y un asiento del mismo “cristal” de que estaban hechas las paredes.

En el asiento, se enroscaba una forma extraña, de contornos vagamente humanos. Observándola de cerca, me pareció, al principio, que se trataba de una estatua deteriorada por la acción del tiempo, pero, luego, descubrí algo que me llenó de horror: bajo el “vidrio” que revestía aquella estatua, ¡se podían distinguir claramente los detalles del esqueleto!”.
Muros, muebles y seres humanos vitrificados… ¿Qué tremendos secretos se esconden entre las líneas del Mahabrata y del Drona Parva?
Emilio Silvera Vázquez
















 Totales: 88.256.722
Totales: 88.256.722 Conectados: 94
Conectados: 94





































