Jul
4
La grasa del Universo
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Astronomía y Astrofísica ~
Clasificado en Astronomía y Astrofísica ~
 Comments (9)
Comments (9)

¿Está el espacio lleno de grasa?
Astrónomos han estimado la cantidad total de cadenas de carbono presentes en el espacio interestelar de la Vía Láctea
El 88 por ciento del espacio interlestelar, la región situada entre las estrellas, está compuesto de átomos de hidrógeno. El 10 por ciento está hecho de helio, y el restante dos por ciento de carbono y oxígeno, así como de otros elementos en menor proporción. La composición de esta sopa permite que se formen moléculas de etanol, agua, dióxido de carbono, metano y amoníaco. Eso sí, su concentración es extraordinariamente baja, así que en realidad no podríamos recoger estas moléculas. Pero, ¿en qué proporción están? ¿Cómo de abundantes son los ingredientes que pueden ser cruciales en la aparición de la vida?

Un estudio recientemente publicado en «Monthly Notices of the Royal Astronomical Society» ha concluido que una gran parte de uno de estos elementos químicos presentes en el espacio interestelar, el carbono, está en forma de moléculas de grasa.
Los investigadores, encabezados por Gunay Banihan, investigador en la Universidad de Turquía, trataron de estimar el contenido de hidrocarburos en el polvo interestelar.

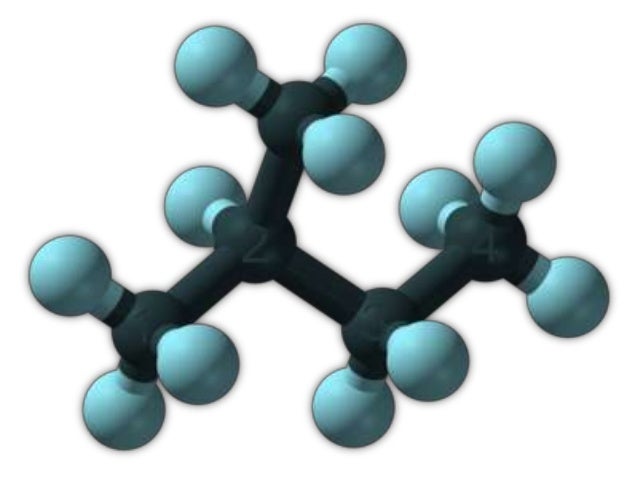
Actualmente, se considera que la mitad del carbono del espacio interestelar está en forma pura, mientras que la otra mitad está en cadenas abiertas (alifáticas) o aromáticas (cerradas, en forma de anillos). Pero se desconoce en qué proporción dichas cadenas tienen una forma u otra.
Los investigadores trataron de crear un polvo con las mismas propiedades del polvo interestelar en el laboratorio. Para ello, recrearon su proceso de formación y sometieron estas moléculas al vacío y a las bajas temperaturas del espacio.
«Combinando nuestros resultados en el laboratorio con las mediciones de observatorios astronómicos, pudimos analizar la cantidad de carbono alifático entre nosotros y las estrellas», ha dicho en Universetoday.com Tim Schmidt, coautor del estudio e investigador en la Universidad de Nueva Gales del Sur (Australia).
A través de estas aproximaciones, los investigadores concluyeron que hay 100 átomos de carbono en forma de grasa por cada millón de átomos de hidrógeno. En la Vía Láctea, eso significaría que hay 10.000 millones de billones de billones de toneladas de grasa.
«¡Esta grasa espacial no es como la que te puedes untar en una tostada! Está sucia, es probablemente tóxica y solo se forma en el espacio interestelar (y en nuestro laboratorio)», ha dicho Schmidt. «Lo que realmente llama la atención es que el material orgánico de este tipo –que luego se incorpora en los sistemas planetarios– sea tan abundante».
A continuación, los investigadores tratarán de estimar la cantidad de carbono aromático, en forma de anillos, que puede existir en el espacio interestelar. En última instancia, estos cálculos permitirán saber cuántos de estos elementos están disponibles en nuestra galaxia y qué implicaciones puede tener esto en la aparición de vida.
Jul
4
Desde los átomos hasta las estrellas: Un largo viaje
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física ~
Clasificado en Física ~
 Comments (0)
Comments (0)
“Pues yo he sido a veces un muchacho y una chica,
Un matorral y un pájaro y un pez en las olas saladas.”
Esto nos decía Empédocles, el padre de aquellos primitivos elementos formados por Agua, tierra, aire y fuego que, mezclados en la debida proporción, formaban todas las cosas que podemos ver a nuestro alrededor. Claro que, él no podía llegar a imaginar hasta donde pudimos llegar después en la comprensión de la materia a partir del descubrimiento de las partículas “elementales” que formaban el átomo. Pero sí, con sus palabras, nos quería decir que, la materia, una veces está conformando mundos y, en otras, estrellas y galaxias.

Sí, hay cosas malas y buenas pero todas deben ser conocidas para poder, en el primer caso aprovecharlas, y en el segundo, prevenirlas.
Pero demos un salto en el tiempo y viajémos hasta los albores del siglo XX cuando se hacía cada vez más evidente que alguna clase de energía atómica era responsable de la potencia del Sol y del resto de las estrellas que más lejos, brillaban en la noche oscura. Ya en 1898, sólo dos años despuès del descubrimiento de la radiactividad por Becquerel, el geólogo americano Thomas Chrowder Chamberlin especulaba que los átomos eran “complejas organizaciones y centros de eneromes energías”, y que “las extraordinarias condiciones que hay en el centro del Sol pueden…liberar una parte de su energía”. Claro que, por aquel entonces, nadie sabía cual era el mecanismo y cómo podía operar, hasta que no llegamos a saber mucho más sobre los átomos y las estrellas.

Conseguimos tener los átomos en nuestras manos
El intento de lograr tal comprensión exigió una colaboración cada vez mayor entre los astrónomos y los físicos nucleares. Su trabajo llevaría, no sólo a resolver la cuestión de la energía estelar, sino también al descubrimiento de una trenza dorada en la que la evolución cósmica se entrelaza en la historia atómica y la estelar.
La Clave: Fue comprender la estructura del átomo. Que el átomo tenía una estructura interna podía inferirse de varias líneas de investigación, entre ellas, el estudio de la radiactividad: para que los átomos emitiesen partículas, como se había hallado que lo hacían en los laboratorios de Becquerel y los Curie, y para que esas emisiones los transformasen de unos elementos en otros, como habían demostrado Rutherford y el químico inglés Frederick Soddy, los átomos debían ser algo más que simples unidades indivisibles, como implicaba su nombre (de la voz griega que significa “imposible de cortar”).
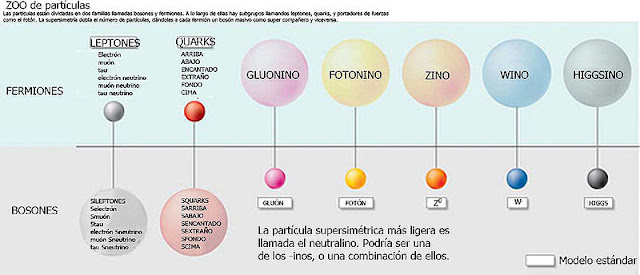
El átomo de Demócrito era mucho más de lo que él, en un principio intuyó que sería. Hoy sabemos que está conformado por diversaspartículas de familias diferentes: unas son bariones que en el seno del átomo llamamos necleones, otras son leptones que gitan alrededor del núcleo para darle estabilidad de cargas, y, otras, de la familia de los Quarks, construyen los bariones del núcleo y, todo ello, está, además, vigilado por otras partículas llamadas bosones intermedios de la fuerza nuclear fuerte, los Gluones que, procuran mantener confinados a los Quarks.
Pero no corramos tanto, la física atómica aún debería recorrer un largo camino para llegar a comprender la estructura que acabamos de reseñar. De los trs principales componentes del átomo -el protón, el neutrón y el electrón-, sólo el electrón había sido identificado (por J.J. Thomson, en los últimos años del siglo XIX). Nadie hablaba de energía “nuclear” pues ni siquiera se había demostrado la existencia de un núcleo atómico, y mucho menos de sus partículas constituyentes, el protón y el neutrón, que serían identificados, respectivamente, por Thomson en 1913 y James Chawick en 1932.

De importancia capital resultó conocer la existencia del núcleo y que éste, era 1/100.000 del total del átomo, es decir, casi todo el átomo estaba compuesto de espacios “vacíos” y, la materia así considerada, era una fracción inifintesimal del total atómico.
Rutherford, Hans Geiger y Ernest Marsden se encontraban entre los Estrabones y Tolomeos de la cartografía atómica, en Manchester , de 1909 a 1911, sonderaron el átomo lanzando corrientes de “partículas alfa” subatómicas -núcleos de helio- contra delgadas laminillas de oro, plata, estaño y otros metales. La mayoría de partículas Alfa se escapaban a través de las laminillas, pero, para sombro de los experimentadores, algunas rebotaban hacia atrás. Rutherford pensó durante largo tiempo e intensamente en este extraño resultado; era tan sorprendente, señalaba, como si una bala rebotase sobre un pañuelo de papel. Finalmente, en una cena en su casa en 1911, anunció a unos pocos amigos que había dado con una explicación: que la mayoría de la masa de un átomo reside en un diminuto núcleo masivo. Ruthertford pudo calcular la carga y el diámetro máximo del nucleo atómico. Así se supo que los elementos pesados eran más pesados que los elementos ligeros porque los núcleos de sus átomos tienen mayor masa.

Todos sabemos ahora, la función que desarrollan los electrones en el atomo. Pero el ámbito de los electrones para poder llegar a la comprensión completa, tuvo que ser explorado, entre otros, por el físico danés Niels Bohr, quien demostró que ocupaban órbitas, o capas, discretas que rodean al núcleo. (Durante un tiempo Bohr consideró el átomo como un diminuto sistema solar, pero ese análisis, pronto demostró ser inadecuado; el átomo no está rígido por la mecánica newtoniana sino por la mecánica cuántica.)
Entre sus muchos otros éxitos, el modelo de Bohr revelaba la base física de la espectroscopia. El número de electrones de un átomo está determinado por la carga eléctrica del núcleo, la que a su vez se debe al número de protones del núcleo, que es la clave de la identidad química del átomo. Cuando un electróncae de una órbita externa a una órbita interior emite un fotón. La longitud de onda de este fotón está determinada por las órbitas particulares entre las que el electrón efectúa la transición. E esta es la razón de que un espectro que registra las longitudes de onda de los fotones, revele los elementos químicos que forman las estrellas u otros objetos que sean estudiados por el espectroscopista. En palabras de Max Planck, el fundador de la física cuántica, el modelo de Bohr del átomo nos proporciona “la llave largamente buscada de la puerta de entrada al maravilloso mundo de la espectroscopia, que desde el descubrimiento del análisis espectral (por Fraunhoufer) había desafiado obtinadamente todos los intentos de conocerlo”.

Es curioso que, mirando en la oscura noche como brillan las estrellas del cielo, nos atrae su titilar engañoso (es la atmósfera terrestre la que hace que lo parezca) y su brillo, Sin embargo, pocos llegan a pensar en lo que verdaderamente está allí ocurriendo. Las transformaciones de fase por fusión no cesan. Esta transformación de materia en energía es consecuencia de la equivalencia materia-energía, enunciada por Albert Einstein en su famosa fórmula E=mc2; donde E es la energía resultante, m es la masa transformada en energía, y c es la velocidad de la luz (300 000 kilómetros por segundo). La cantidad de energía que se libera en los procesos de fusión termonuclear es fabulosa. Un gramo de materia transformado íntegramente en energía bastaría para satisfacer los requerimientos energéticos de una familia mediana durante miles de años.
Es un gran triunfo del ingenio humano el saber de qué, están confomadas las estrellas, de qué materiales están hechas. Recuerdo aquí a aquel Presidente de la Real Society de Londres que, en una reunión multitudinaria, llegó a decir: “Una cosa está clara, nunca podremos saber de qué están hechas las estrellas”. El hombre se vistió de gloria con la, desde entonces, famosa frase. Creo que nada, con tiempo por delante, será imposible para nosotros.
Pero, por maravilloso que nos pueda parecer el haber llegado a la comprensión de que los espectros revelan saltos y tumbos de los electrones en sus órbitas de Bohr, aún nadie podía hallar en los espectros de las estrellas las claves significativas sobre lo que las hace brillar. En ausencia de una teoría convincente, se abandonó este campo a los taxonomistas, a los que seguían obstinadamente registrando y catalogando espectros de estrellas, aunque no sabían hacia donde los conduciría esto.
En el Laboratorio de la Universidad de Harvard, uno de los principales centros de la monótona pero prometedora tarea de la taxonomía estelar, las placas fotográficas que mostraban los colores y espectros de decenas de miles de estrellas se apilaban delante de “calculadoras”, mujeres solteras en su mayoría y, de entre ellas, Henrietta Leavitt, la investigadora pionera de las estrellas variables Cefeidas que tan útiles serían a Shapley y Hubble.

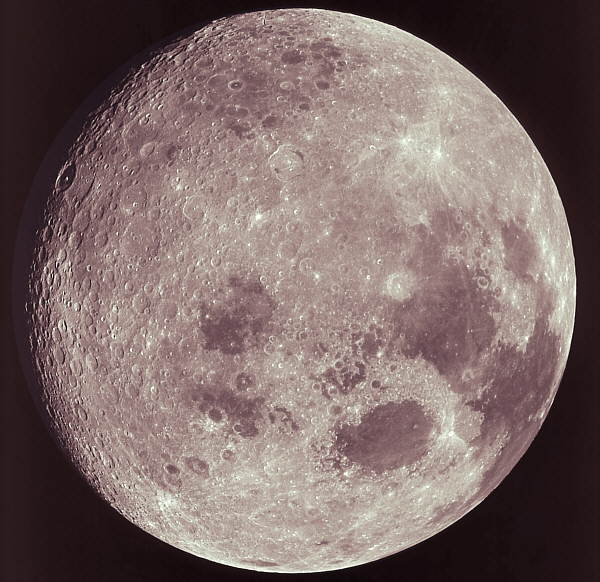
Imagen de Sirio A, la estrella más brillante del cielo tomada por el Telescopio Hubble (Créd. NASA). Sirio es la quinta estrella más cercana y tiene una edad de 300, millones de años. Es una estrella blanca de la secuencia principal de tipo espectral A1V con temperatura superficial de 10 000 K y situada a 8,6 años luz de la Tierra. Es una estrella binaria y, de ella, podríamos contar muchas historias. La estrella fue importante en las vidas de Civilizaciones pasadas como, por ejemplo, la egipcia.
Fue Cannon quien, en 1915, empezó a discernir la forma en una totalidad de estrellas en las que estaba presente la diversidad, cuando descubrió que en una mayoría, las estrellas, pertenecían a una de media docena de clases espectrales distintas. Su sistema de clasificación, ahora generalizado en la astronomía estelar, ordena los espectros por el color, desde las estrellas O blancoazuladas, pasando por las estrellas G amarillas como el Sol, hasta estrellas rojas M. Era un rasgo de simplicidad denajo de la asombrosa variedad de las estrellas.
Pronto se descubrió un orden más profundo, en 1911, cuando el ingeniero y astrónomo autodidacta danés Ejnar Hertzsprung analizó los datos de Cannon y Maury de las estrellas de dos cúmulos, las Híades y las Pléyades. Los cúmulos como estos son genuinos conjuntos de estrellas y no meras alineaciones al azar; hasta un observador inexperimentado salta entusiamado cuando recorre con el telecopio las Pléyades, con sus estrellas color azul verdoso enredadas en telarañas de polvo de diamante, o las Híades, cuyas estrellas varían en color desde el blanco mate hasta un amarillo apagado.

Las Híades
Hertzsprung utilizó los cúmulos como muestras de laboratorio con las que podía buscar una relación entre los colores y los brillos intrínsecos de las estrellas. Halló tal relación: la mayoría de las estrellas de ambos cúmulos caían en dos líneas suavemente curvadas. Esto, en forma de gráfico, fue el primer esbozo de un árbol de estrellas que desde entonces ha sido llamado diagrama Hertzsprung-Russell.
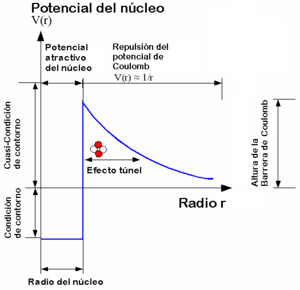
El progreso en física, mientras tanto, estaba bloquedado por una barrera aparentemente insuperable. Esto era literal: el agente responsable era conocido como barrera de Coulomb, y por un tiempo frustó los esfuerzos de las físicos teóricos para copmprender como la fusión nuclear podía producir energía en las estrellas.
La línea de razonamiento que conducía a esa barrera era impecable. Las estrellas están formadas en su mayor parte por hidrógeno. (Esto se hace evidente en el estudio de sus espectros.) El núcleo del átomo de Hidrógeno consiste en un solo protón, y el protón contiene casi toda la masa del átomo. (Sabemos esto por los experimentos de Rutherford). Por tanto, el protón también debe contener casi toda la energía latente del átomo de hidrógeno. (Recordemos que la masa es igual a la energía: E = mc2.) En el calor de una estrella, los protones son esparcidos a altas velocidades -el calor intenso significa que las partículas involucradas se mueven a enormes velocidades- y, como hay muchos protones que se apiñan en el núcleo denso de una estrella, deben tener muchísimos choques. En resumen, la energía del Sol y las estrellas, puede suponerse razonablemente, implica las interacciones de los protones. Esta era la base de la conjetura de Eddintong de que la fuente de la energía estelar “difícilmente puede ser otra que la energía subatómica, la cual, como se sabe, existe en abundancia en toda materia”.

Plasma en ebullición en la superficie del Sol
Hasta el momento todo lo que hemos repasado está bien pero, ¿que pasa con la Barrera de Coulomb? Los protones están cargados positivamente; las partículasd de igual carga se repelen entre sí; y este obstáculo parecía demasiado grande para ser superado, aun a la elevada velocidad a la que los protones se agitaban en el intenso calor del interior de las estrellas. De acuerdo con la física clásica, muy raras veces podían dos protones de una estrella ir con la rapidez suficiente para romper las murallas de sus campos de fuerza electromagnéticos y fundirse en un solo núcleo. Los cálculos decían que la tasa de colisión de protones no podía bastar para mantener las reacciones de fusión. Sin embargo, allí estaba el Sol, con el rostro radiante, riéndose de las ecuaciones que afirmaban que no podía brillar.
Afortunadamente, en el ámbito nuclear, las reglas de la Naturaleza no se rigen por las de la mecánica de la física clásica, que tienen validez para grandes objetos, como guijarros y planetas, pero pierden esa validez en el reino de lo muy pequeño. En la escala nuclear, rigen las reglas de la indeterminación cuántica. La mecánica cuántica demuestra que el futuro del protón sólo puede predecirse en términos de probabilidades: la mayoría de las veces el protón rebotará en la Barrera de Coulomb, pero de cuando en cuando, la atravesará. Este es el “efecto túnel cuántico”; que permite brillar a las estrellas.

George Gamow, ansioso de explotar las conexiones entre la astronomía y la nueva física exótica a la que era adepto, aplicó las probabilidades cuánticas a la cuestión de la fusión nuclear en las estrellas y descubrió que los protones pueden superar la Barrera de Coulomb. Esta historia es mucho más extensa y nos llevaría hasta los trabajos de Hans Bethe, Edward Teller y otros, así como, al famoso Fred Hoyle y su efecto Triple Alfa y otras maravillas que, nos cuentan la historia que existe desde los átomos a las estrellas del cielo.
emilio silvera















 Totales: 67.202.605
Totales: 67.202.605 Conectados: 45
Conectados: 45






















