Nov
23
¡Los materiales para la vida! Y, de los mundos
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en El Universo y la Química de la Vida ~
Clasificado en El Universo y la Química de la Vida ~
 Comments (0)
Comments (0)

¿Será así la espuma cuántica?
Los elementos se crean en las estrellas y en las explosiones supernovas
¡La Física! Cuando se asocia a otras disciplinas ha dado siempre un resultado espectacular y, en el caso de la Astronomía, cuando se juntó con la Física, surgió esa otra disciplina que llamamos Astrofísica. La Astrofísica es esa nueva rama de la Astronomía que estudia los procesos físicos y químicos en los que intervienen los fenómenos astronómicos. La Astrofísica se ocupa de la estructura y evolución estelar (incluyendo la generación y transporte de energía en las estrellas), las propiedades del medio interestelar y sus interacciones en sus sistemas estelares y la estructura y dinámica de los sistemas de estrellas (como cúmulos y galaxias) y sistemas de galaxias. Se sigue con la Cosmología que estudia la naturaleza, el origen y la evolución del universo. Existen varias teorías sobre el origen y evolución del universo (big bang, teoría del estado estacionario, etc.

Las estrellas, como todo en el Universo, no son inmutables y, con el paso del Tiempo, cambian para convertirse en objetos diferentes de los que, en un principio eran. Por el largo trayecto de sus vidas, transforman los materiales simples en materiales complejos sobre los que se producen procesos biológico-químicos que, en algunos casos, pueden llegar hasta la vida.
Una de las cosas que siempre me han llamado poderosamente la atención, han sido las estrellas y las transformaciones que, dentro de ellas y los procesos que en su interior se procesan, dan lugar a las transiciones de materiales sencillos hacia materiales más complejos y, finalmente, cuando al final de sus vidas expulsan las capas exteriores al espacio interestelar dejando una extensa región del espacio interestelar sembrada de diversas sustancias que, siguiendo los procesos naturales e interacciones con todo lo que en el lugar está presente, da lugar a procesos químicos que transforman esas sustancias primeras en otras más complejas, sustancias orgánicas simples como, hidrocarburos y derivados que, finalmente, llegan a ser los materiales necesarios para que, mediante la química-biológica del espacio, den lugar a moléculas y sustancias que son las propicias para hacer posible el surgir de la vida.


La Química de los Carbohidratos es una parte de la Química Orgánica que ha tenido cierta entidad propia desde los comienzos del siglo XX, probablemente debido a la importancia química, biológica (inicialmente como sustancias de reserva energética) e industrial (industrias alimentaria y del papel) de estas sustancias. Ya muy avanzada la segunda mitad del siglo XX han ocurrido dos hechos que han potenciado a la Química de Carbohidratos como una de las áreas con más desarrollo dentro de la Química Orgánica actual.
Todos los animales, plantas y microbios están compuestos fundamentalmente, por las denominadas sustancias orgánicas. Sin ellas, la vida no tiene explicación (al menos que sepamos). De esta manera, en el primer período del origen de la vida tuvieron que formarse dichas sustancias, o sea, surgimiento de la materia prima que más tarde serviría para la formación de los seres vivos.

La característica principal que diferencia a las sustancias orgánicas de las inorgánicas, es que en el contenido de las primeras se encuentra como elemento fundamental el Carbono.
En las sustancias orgánicas, el carbono se combina con otros elementos: hidrógeno y oxígeno (ambos elementos juntos forman agua), nitrógeno (este se encuentra en grandes cantidades en el aire, azufre, fósforo, etc. Las distintas sustancias orgánicas no son más que las diferentes combinaciones de los elementos mencionados, pero en todas ellas, como elemento básico, siempre está el Carbono.
En el primer nivel (abajo) están los productores, o sea las plantas como maíz, frijol, papaya, cupesí, mora, yuca, árboles, hierbas, lianas, etc., que producen hojas, frutas, raíces, semillas, que comen varios animales y la gente.
En el segundo nivel están los primeros consumidores, que comen hierbas, hojas (herbívoros) y frutas (frugívoros). Estos primeros consumidores incluyen a insectos como hormigas, aves como loros y mamíferos como ratones, urina, chanchos, chivas, vacas.

En el tercer nivel están los segundos consumidores (carnívoros), es decir los que se comen a los animales del segundo nivel: por ejemplo el oso bandera come hormigas, el jausi (lagarto terrestre sudamericano), come insectos y la culebra come ratones.
Nosotros, los humanos, somos omnívoros, es decir comemos de todo: plantas y animales. Algunos de los carnívoros comen, a veces, plantas también, como los perros. Otros, como el chancho, comen muchas plantas y a veces también carne.
Las sustancias orgánicas más sencillas y elementales son los llamados hidrocarburos o composiciones donde se combinan el Oxígeno y el Hidrógeno. El petróleo natural y otros derivados suyos, como la gasolina, el keroseno, etc., son mezcolanzas de varios hidrocarburos. Con todas estas sustancias como base, los químicos obtienen sin problemas, por síntesis, gran cantidad de combinados orgánicos, en ocasiones muy complejos y otras veces iguales a los que tomamos directamente los seres vivos, como azúcares, grasas, aceites esenciales y otros. Debemos preguntarnos como llegaron a formarse en nuestro planeta las sustancias orgánicas.
Está claro que, para los iniciados en estos temas, la cosa puede parecer de una complejidad inalcanzable, nada menos que llegar a comprender ¡el origen primario de las sustancias orgánicas!
Es nuestro planeta y el único habitado (hasta donde podemos saber). Está en la ecos-fera, un espacio que rodea al Sol y que tiene las condiciones necesarias para que exista vida. Claro que, ¡son tantos los mundos! Cómo vamos a ser nosotros nos únicos que poblemos el Universo? ¡Que desperdicio de espacio!

La observación directa de la Naturaleza que nos rodea nos puede facilitar las respuestas que necesitamos. En realidad, si ahora comprobamos todas las sustancias orgánicas propias de nuestro mundo en relación a los seres vivos podemos ver que, todas, son producidas hoy día en la Tierra por efecto de la función activa y vital de los organismos.
Las plantas verdes absorben el carbono inorgánico del aire, en calidad de anhídrido carbónico, y con la energía de la luz crean, a partir de éste, sustancias orgánicas necesarias para ellas. Los animales, los hongos, también las bacterias y el resto de organismos, menos los de color verde, se alimentan de animales o vegetales vivos o descomponiendo estos mismos, una vez muertos, pueden proveerse de las sustancias orgánicas que necesitan. Con esto, podemos ver como todo el mundo actual de los seres vivos depende de los dos hechos análogos de fotosíntesis y quimio-síntesis, aplicados en las líneas anteriores.
Incluso las sustancias orgánicas que se encuentran bajo tierra como la turba, la hulla o el petróleo, han surgido, básicamente, por efecto de la acción de diferentes organismos que en un tiempo remoto se encontraban en el planeta Tierra y que con el transcurrir de los siglos quedaron ocultos bajo la maciza corteza terrestre.
Todo esto fue causa de que muchos científicos de finales del siglo XIX y principios del XX, afirmaran que era imposible que las sustancias orgánicas produjeran en la Tierra, de forma natural, solamente mediante un proceso biogenético, o sea, con la única intervención de los organismos. Esta opinión predominante entre los científicos de hace algunas décadas, constituyó un obstáculo considerable para hallar una respuesta a la cuestión del origen de la vida.

Para que todo fuese posible, se necesitaba una atmósfera favorable
Para tratar esta cuestión era indispensable saber cómo llegaron a constituirse las sustancias orgánicas; pero ocurría que éstas sólo podían ser sintetizadas por organismos vivos. Sin embargo, únicamente podemos llegar a esta síntesis si nuestras observaciones no van más allá de los límites del planeta Tierra. Si traspasamos esa frontera nos encontraremos con que en diferentes cuerpos celestes de nuestra Galaxia se están creando sustancias orgánicas de manera a-biogenética, es decir, en un ambiente que excluye cualquier posibilidad de que existan seres orgánicos en aquel lugar.
Estrella de carbono (estrella gigante roja)
Con un espectroscopio podemos estudiar la fórmula química de las atmósferas estelares, y en ocasiones casi con la misma exactitud que si tuviéramos alguna muestra de éstas en el Laboratorio. El Carbono, por ejemplo, se manifiesta ya en las atmósferas de las estrellas tipo O, que son las que están a mayor temperatura, y su increíble brillo es lo que las diferencia de los demás astros (Ya os hablé aquí de R. Lepori, la estrella carmesí, o, también conocida como la Gota de Sangre, una estrella de Carbono de increíble belleza).
En la superficie de las estrellas de Carbono existe una temperatura que oscila los 20.000 y los 28.000 grados. Es comprensible, entonces, que en esa situación no pueda prevalecer aún alguna combinación química. La materia está aquí en forma relativamente simple, como átomos libres disgregados, sueltos como partículas minúsculas que conforman la atmósfera incandescente de estos cuerpos estelares.

La atmósfera de las estrellas tipo B, característica por su luz brillante blanco-azulada y cuya corteza tiene una temperatura que va de 15.000 a 20.000 grados, también tienen vapores incandescentes de carbono. Pero aquí este elemento tampoco puede formar cuerpos químicos compuestos, únicamente existe en forma atómica, o sea, en forma de pequeñísimas partículas sueltas de materia que se mueven a una velocidad de vértigo.

Sólo la visión espectral de las estrellas Blancas tipo A, en cuya superficie hay una temperatura de unos 12.000º, muestras unas franjas tenues, que indican, por primera vez, la presencia de hidrocarburos –las más primitiva combinaciones químicas de la atmósfera de estas estrellas. Aquí, sin que existan antecedentes, los átomos de dos elementos (el carbono y el hidrógeno) se combinan resultando un cuerpo más perfecto y complejo, una molécula química.
Observando las estrellas más frías, las franjas características de los hidrocarburos son más limpias cuando más baja es la temperatura y adquieren su máxima claridad en las estrellas rojas, en cuya superficie la temperatura nunca es superior a los 4.000º.
Es curioso el resultado obtenido de la medición de Carbono en algunos cuerpos estelares por su temperatura:
- Proción: 8.000º
- Betelgeuse: 2.600º
- Sirio: 11.000º
- Rigel: 20.000º
Como es lógico pensar, las distintas estrellas se encuentran en diferentes períodos de desarrollo. El Carbono se encuentra presente en todas ellas, pero en distintos estados del mismo.
Las estrellas más jóvenes, de un color blanco-azulado son a la vez las más calientes. Éstas poseen una temperatura muy elevada, pues sólo en la superficie se alcanzan los 20.000 grados.


Los científicos descubrieron una enorme cantidad de silicatos cristalinos e hidrocarburos policíclicos aromáticos, dos sustancias que indican la presencia de oxígeno y de carbono, respectivamente. Así todos los elementos que las componen, incluido el Carbono, están en forma de átomos, de diminutas partículas sueltas. Existen estrellas de color amarillo y la temperatura en su superficie oscila entre los 6.000 y los 8.000º. En estas también encontramos Carbono en diferentes combinaciones.
El Sol, pertenece al grupo de las estrellas amarillas y en la superficie la temperatura es de 6.000º. El Carbono en la atmósfera incandescente del Sol, lo encontramos en forma de átomo, y además desarrollando diferentes combinaciones: Átomos de Carbono, Hidrógeno y Nitrógeno, Metino, Cianógeno, Dicaerbono, es decir:
- Átomos sueltos de Carbono, Hidrógeno y Nitrógeno.
- Miscibilidad combinada de carbono e hidrógeno (metano)
- Miscibilidad combinada de carbono y nitrógeno (cianógeno); y
- Dos átomos de Carbono en combinación (di-carbono).
En las atmósferas de las estrellas más calientes, el carbono únicamente se manifiesta mediante átomos libres y sueltos. Sin embargo, en el Sol, como sabemos, en parte, se presenta ya, formando combinaciones químicas en forma de moléculas de hidrocarburo de cianógeno y de di-carbono.

Para hallar las respuestas que estamos buscando en el conocimiento de las sustancias y materiales presentes en los astros y planetas, ya se está realizando un estudio en profundidad de la atmósfera de los grandes planetas del Sistema solar. Y, de momento, dichos estudios han descubierto, por ejemplo, que la atmósfera de Júpiter está formada mayoritariamente por amoníaco y metano. Lo cual hace pensar en la existencia de otros hidrocarburos. Sin embargo, la masa que forma la base de esos hidrocarburos, en Júpiter permanece en estado líquido o sólido a causa de la abaja temperatura que hay en la superficie del planeta (135 grados bajo cero). En la atmósfera del resto de grandes planetas se manifiestan estas mismas combinaciones.
Ha sido especialmente importante el estudio de los meteoritos, esas “piedras celestes” que caen sobre la Tierra de vez en cuando, y que provienen del espacio interplanetario. Estos han representado para los estudiosos los únicos cuerpos extraterrestres que han podido someter a profundos análisis químico y metalúrgico, de forma directa. Sin olvidar, en algunos casos, los posibles fósiles.
Estos meteoritos están compuestos del mismo material que encontramos en la parte más profunda de la corteza del planeta Tierra y en su núcleo central, tanto por el carácter de los elementos que los componen como por la base de su estructura. Es fácil entender la importancia capital que tiene el estudio de los materiales de estas piedras celestes para resolver la cuestión del origen de las primitivas composiciones durante el período de formación de nuestro planeta que, al fin y al cabo, es la misma que estará presente en la conformación de otros planetas rocosos similares al nuestro, ya que, no lo olvidemos, en todo el universo rigen las mismas leyes y, la mecánica de los mundos y de las estrellas se repiten una y otra vez aquí y allí, a miles de millones de años-luz de nosotros.
Así que, se forman hidrocarburos al contactar los carburos con el agua. Las moléculas de agua contienen oxígeno que, combinado con el metal, forman los hidróxidos metálicos, mientras que el hidrógeno del agua mezclado con el carbono forman los hidrocarburos.
Los hidrocarburos originados en la atmósfera terrestre se mezclaron con las partículas de agua y amoníaco que en ella existían, creando sustancias más complejas. Así, llegaron a hacerse presentes la formación de cuerpos químicos. Moléculas compuestas por partículas de oxígeno, hidrógeno y carbono.
Todo esto desembocó en el saber sobre los Elementos que hoy podemos conocer y, a partir de Mendeléiev (un eminente químico ruso) y otros muchos…se hizo posible que el estudio llegara muy lejos y, al día de hoy, podríamos decir que se conocen todos los elementos naturales y algunos artificiales que, nos llevan a tener unos valiosos datos de la materia que en el universo está presente y, en parte, de cómo funciona cuando, esas sustancias o átomos, llegan a ligarse los unos con los otros para formar, materiales más complejos que, aparte de los naturales, están los artificiales o transuránicos.
Aquí en la Tierra, las reacciones de hidrocarburos y sus derivados oxigenados más simples con el amoníaco generaron otros cuerpos con distintas combinaciones de átomos de carbono, hidrógeno, oxígeno y nitrógeno (CHON) en su moléculas llamadas paras la vida una vez que, más tarde, por distintos fenómenos de diversos tipos, llegaron las primeras sustancias proteínicas y grasas que, dieron lugar a los aminoácidos, las Proteínas y el ADN y RDN que, finalmente desembocó en eso que llamamos vida y que, evolucionado, ha resultado ser tan complejo y, a veces, en ciertas circunstancias, peligroso: ¡Nosotros!
Emilio Silvera V.
Nov
23
Los secretos del Universo y, de la vida.
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en General ~
Clasificado en General ~
 Comments (0)
Comments (0)
Habiendo repasado uno de los trabajos que se pusieron días pasados, me ha parecido que no está completo y aquí lo arreglo y lo dejo de manera más amplia para que todos puedan entender el mensaje.


Paul Dirac ocupó la cátedra lucasiana de matemáticas en Cambridge durante parte del tiempo en que Eddington estuvo viviendo en los observatorios. Las historias que se cuentan de Paul Dirac dejan muy claro que era un tipo con un carácter peculiar, y ejercía de matemático las 24 h. del día. Se pudo saber que su inesperada incursión en los grandes números fue escrita durante su viaje de novios (Luna de miel), en febrero de 1.937.
Aunque no muy convencido de las explicaciones de Eddington, escribió que era muy poco probable que números adimensionales muy grandes, que toman valores como 1040 y 1080, sean accidentes independientes y no relacionados: debe existir alguna fórmula matemática no descubierta que liga las cantidades implicadas. Deben ser consecuencias más que coincidencias.
Aquí tenéis la hipótesis de los grandes números según Dirac:
“Dos cualesquiera de los números adimensionales muy grandes que ocurren en la naturaleza están conectados por una sencilla relación matemática, en la que los coeficientes son del orden de la unidad”.
Los grandes números de que se valía Dirac para formular esta atrevida hipótesis salían del trabajo de Eddington y eran tres:
N1 = (tamaño del universo observable) / (radio del electrón) = ct (e2/mec2) ≈ 1040
N2 = Razón fuerza electromagnética-a-gravitatoria entre protón y electrón = e2/Gme mp ≈ 1040
N = número de protones en el universo observable = c3t/Gmp ≈ 1080
Aquí t es la edad actual del universo, me es la masa de un electrón, mp es la masa de un protón, G la constante de gravitación, c la velocidad de la luz y e la carga del electrón.
Según la hipótesis de Dirac, los números N1, N2y √N eran realmente iguales salvo pequeños factores numéricos del orden de la unidad. Con esto quería decir que debe haber leyes de la naturaleza que exijan fórmulas como N1 = N2, o incluso N1 = 2N2. Un número como 2 ó 3, no es terriblemente diferente de 1 está permitido porque es mucho más pequeño que los grandes números implicados en la fórmula; esto es lo que él quería decir por “coeficientes…. del orden de la unidad”.
Esta hipótesis de igualdad entre grandes números no era en sí misma original de Dirac. Eddington y otros habían escrito antes relaciones muy semejantes, pero Eddington no había distinguido entre el número de partículas del universo observable, que se define como una esfera centrada en nosotros con un radio igual a la velocidad de la luz multiplicada por la edad actual del universo, o lo que es lo mismo:
Universo observable: R = 300.000 × 13.500.000.000
El cambio radical expuesto por Dirac en su hipótesis de grandes números es que nos exige que creamos que un conjunto de constantes tradicionales de la naturaleza, como N2, debe estar cambiando a medida que el universo envejece en el tiempo, t:
N1 ≈ N2 ≈ √N ≡ t
Puesto que Dirac había incluido dos combinaciones que contenían la edad del universo, t, en su catálogo de grandes números, la relación que él propone requiere que una combinación de tres de las constantes de la naturaleza tradicionales no sea constante en absoluto, sino que su valor debe aumentar continuamente a medida que el universo se hace más viejo, de modo que
e2/Gmp ≡ t
Dirac decidió acomodar este requisito abandonando la constancia de la constante de gravitación de Newton, G. Sugirió que estaba decreciendo en proporción directa a la edad del universo en escalas de tiempo cósmicas, como
G ≡ 1/t
Así pues, en el pasado G era mayor y en el futuro será menor que lo que mide hoy. Ahora veremos que N1 ≈ N2 ≈ √N ≡ t y la enorme magnitud de los tres grandes números es una consecuencia de la gran edad del universo: todas aumentan con el paso del tiempo.
La propuesta de Dirac provocó un revuelo entre un grupo de científicos vociferantes que inundaron las páginas de las revistas especializadas de cartas y artículos a favor y en contra. Dirac, mientras tanto, mantenía su calma y sus tranquilas costumbres, pero escribió sobre su creencia en los grandes números cuya importancia encerraba la comprensión del universo con palabras que podrían haber sido de Eddington, pues reflejan muy estrechamente la filosofía de la fracasada “teoría fundamental”.
“¿No cabría la posibilidad de que todos los grandes sucesos presentes correspondan a propiedades de este Gran Número [1040] y, generalizando aún más, que la historia entera del universo corresponda a propiedades de la serie entera de los números naturales…? Hay así una posibilidad de que el viejo sueño de los filósofos de conectar la naturaleza con las propiedades de los números enteros se realice algún día”.
La propuesta de Dirac levantó controversias entre los físicos, y Edward Teller en 1.948, demostró que si en el pasado la gravedad hubiera sido como dice Dirac, la emisión de la energía del Sol habría cambiado y la Tierra habría estado mucho más caliente en el pasado de lo que se suponía normalmente, los océanos habrían estado hirviendo en la era precámbrica, hace doscientos o trescientos millones de años, y la vida tal como la conocemos no habría sobrevivido, pese a que la evidencia geológica entonces disponible demostraba que la vida había existido hace al menos quinientos millones de años.
El eufórico George Gamow era buen amigo de Teller y respondió al problema del océano hirviente sugiriendo que podía paliarse si se suponía que las coincidencias propuestas por Dirac eran debidas a una variación temporal en e, la carga del electrón, con e2 aumentando con el tiempo como requiere la ecuación e2/Gmp ≡ t
Por desgracia, la propuesta de Gamow de una e variable tenía todo tipo de consecuencias inaceptables para la vida sobre la Tierra. Pronto se advirtió que la sugerencia de Gamow hubiera dado como resultado que el Sol habría agotado hace tiempo todo su combustible nuclear, no estaría brillando hoy si e2 crece en proporción a la edad del universo. Su valor en el pasado demasiado pequeño habría impedido que se formaran estrellas como el Sol. Las consecuencias de haber comprimido antes su combustible nuclear, el hidrógeno, hubiera sido la de convertirse primero en gigante roja y después en enana blanca y, por el camino, en el proceso, los mares y océanos de la Tierra se habrían evaporado y la vida habría desaparecido de la faz del planeta.
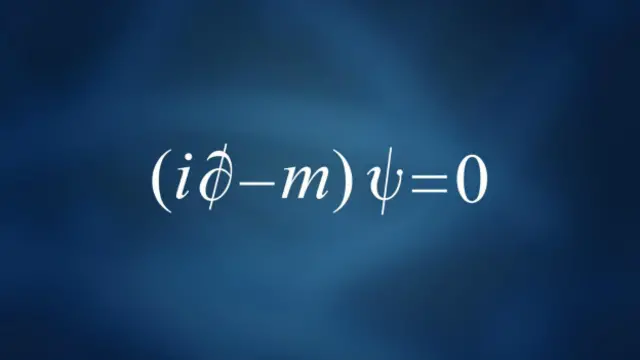
Dirac describió el electrón incluyendo la relatividad y su formula es de una gran belleza
Gamow tuvo varias discusiones con Dirac sobre estas variantes de su hipótesis de G variable. Dirac dio una interesante respuesta a Gamow con respecto a su idea de la carga del electrón, y con ello la constante de estructura fina, pudiera estar variando.
Recordando sin duda la creencia inicial de Eddington en que la constante de estructura fina era un número racional, escribe a Gamow en 1.961 hablándole de las consecuencias cosmológicas de su variación con el logaritmo de la edad del universo.

La Constante de estructura fina 1/137
“Es difícil formular cualquier teoría firme sobre las etapas primitivas del universo porque no sabemos si hc/e2 es constante o varía proporcionalmente a log(t). Si hc/e2 fuera un entero tendría que ser una constante, pero los experimentadores dicen ahora que no es un entero, de modo que bien podría estar variando. Si realmente varía, la química de las etapas primitivas sería completamente diferente, y la radiactividad también estaría afectada. Cuando empecé a trabajar sobre la gravedad esperaba encontrar alguna conexión entre ella y los neutrinos, pero esto ha fracasado.”
Dirac no iba a suscribir una e variable fácilmente, como solución al problema de los grandes números. Precisamente, su trabajo científico más importante había hecho comprensible la estructura de los átomos y el comportamiento del electrón, y dijo que existía el positrón. Todo ello basado en la hipótesis, compartida por casi todos, de que e era una verdadera constante, la misma en todo tiempo y todo lugar en el universo, un electrón y su carga negativa eran exactas en la Tierra y en el más alejado planeta de la más alejada estrella de la galaxia Andrómeda. Así que Gamow pronto abandonó la teoría de la e variable y concluyo que:

“El valor de e se mantiene en pie como el Peñón de Gibraltar durante los últimos 6×109 años.”
Pero lo que está claro es que, como ocurre siempre en ciencia, la propuesta de Dirac levantó una gran controversia que llevó a cientos de físicos a realizar pruebas y buscar más a fondo en el problema, lo que dio lugar a nuevos detalles importantes sobre el tema.

Alain Turing, pionero de la criptografía, estaba fascinado por la idea de la gravedad variable de Dirac, y especuló sobre la posibilidad de probar la idea a partir de la evidencia fósil, preguntando si “un paleontólogo podría decir, a partir de la huella de un animal extinto, si su peso era el que se suponía”.
El gran biólogo J.B.S. Haldane se sintió también atraído por las posibles consecuencias biológicas de las teorías cosmológicas en que las “constantes” tradicionales cambian con el paso del tiempo o donde los procesos gravitatorios se despliegan de acuerdo con un reloj cósmico diferente del de los procesos atómicos (¿será precisamente por eso que la relatividad general – el cosmos -, no se lleva bien con la mecánica cuántica – el átomo -?).
Tales universos de dos tiempos habían sido propuestos por Edward Arthur Milne y fueron las primeras sugerencias de que G podría no ser constante. Unos procesos, como la desintegración radiactiva o los ritmos de interacción molecular, podrían ser constantes sobre una escala de tiempo pero significativamente variables con respecto a la otra. Esto daba lugar a un escenario en el que la bioquímica que sustentaba la vida sólo se hacía posible después de una particular época cósmica, Haldane sugiere que:
“Hubo, de hecho, un momento en el que se hizo posible por primera vez vida de cualquier tipo, y las formas superiores de vida sólo pueden haberse hecho posibles en una fecha posterior. Análogamente, un cambio en las propiedades de la materia puede explicar algunas de las peculiaridades de la geología precámbrica.”
Este imaginativo escenario no es diferente del que ahora se conoce como “equilibrio interrumpido”, en el que la evolución ocurre en una sucesión discontinua de brotes acelerados entre los que se intercalan largos periodos de cambio lento. Sin embargo, Haldane ofrece una explicación para los cambios.
Lo que tienen en común todas estas respuestas a las ideas de Eddington y Dirac es una apreciación creciente de que las constantes de la naturaleza desempeñan un papel cosmológico vital:
Existe un lazo entre la estructura del universo en conjunto y las condiciones locales internas que se necesitan para que la vida se desarrolle y persista. Si las constantes tradicionales varían, entonces las teorías astronómicas tienen grandes consecuencias para la biología, la geología y la propia vida.

Si la carga del electrón o la masa del protón (dos constantes de la Naturaleza), cariaran aunque solo fuese unas diez millonésimas… ¡Los átomos no se podrían formar y, la vida, no hubiera podido surgir.
No podemos descartar la idea ni abandonar la posibilidad de que algunas “constantes” tradicionales de la naturaleza pudieran estar variando muy lentamente durante el transcurso de los miles de millones de años de la historia del universo. Es comprensible por tanto el interés por los grandes números que incluyen las constantes de la naturaleza. Recordemos que Newton nos trajo su teoría de la Gravedad Universal, que más tarde mejora Einstein y que, no sería extraño, en el futuro mejorará algún otro con una nueva teoría más completa y ambiciosa que explique lo grande (el cosmos) y lo pequeño (el átomo), las partículas (la materia) y la energía por interacción de las cuatro fuerzas fundamentales.

La teoría de cuerdas podría permitir pequeñas “vibraciones de Lorentz”, que son derivaciones de la invariancia de Lorentz, un principio fundamental de la relatividad que postula que las leyes de la física son las mismas para todos los observadores inerciales. Estas violaciones serían muy pequeñas y solo se manifestarían en energías muy altas o a escalas muy pequeñas, por lo que son difíciles de detectar experimentalmente.


¿Será la teoría de Supercuerdas ese futuro?
Robert Dicke
Me referiré ahora aquí a un físico extraño. Se sentía igualmente cómodo como matemático, como físico experimental, como destilador de datos astronómicos complicados o como diseñador de sofisticados instrumentos de medida.
Tenía los intereses científicos más amplios y diversos que imaginarse pueda. Él decía que al final del camino todos los conocimientos convergen en un solo punto, el saber.
Así de curioso, ya podéis imaginar que fue uno de los que de inmediato se puso manos a la obra para comprobar la idea de la constante gravitatoria variable de Dirac que podía ser sometida a una gran cantidad de pruebas observacionales, utilizando los datos de la geología, la paleontología, la astronomía, la física de laboratorio y cualquier otro que pudiera dar una pista sobre ello. No estaba motivado por el deseo de explicar los grandes números. Hacia mediados de la década de los 60 hubo una motivación adicional para desarrollar una extensión de la teoría de la gravedad de Einstein que incluye una G variable. En efecto, durante un tiempo pareció que las predicciones de Einstein no coincidían en lo referente o sobre el cambio de órbita de Mercurio que era distinta a las observaciones cuando se tenía en cuenta la forma ligeramente achatada del Sol.
Robert Dicke, que este era el nombre del extraño personaje, y su estudiante de investigación Carl Brans, en 1.961, demostraron que si se permitía una variación de G con el tiempo, entonces podía elegirse un ritmo de cambio para tener un valor que coincidiera con las observaciones de la órbita de Mercurio. Lamentablemente, se descubrió que todo esto era una pérdida de tiempo. El desacuerdo con la teoría de Einstein a inexactitudes de nuestros intentos de medir el diámetro del Sol que hacían que este pareciera tener una forma de órbita diferente a la real. Con su turbulenta superficie, en aquel tiempo, no era fácil medir el tamaño del Sol. Así que, una vez resuelto este problema en 1.977, desapareció la necesidad de una G variable para conciliar la observación con la teoría.
Curiosidades
Lo cierto es que, los grandes números del Universo, nada tiene que ver con la Lotería. Están ahí porque tienen que estar. Otra cuestión será que nosotros no sepamos por qué.
De todas las maneras, lo anterior no quita importancia al trabajo realizado por Dicke que preparó una revisión importante de las evidencias geofísicas, paleontológicas y astronómicas a favor de posibles variaciones de las constantes físicas tradicionales. Hizo la interesante observación de explicar los “grandes números” de Eddington y Dirac bajo el apunte de que allí tenía que subyacer algún aspecto biológico que de momento no éramos capaces de ver.
“El problema del gran tamaño de estos números es ahora fácil de explicar… Hay un único número adimensional grande que tiene su origen estático. Este es el número de partículas del universo. La edad del universo “ahora” no es aleatoria sino que está condicionada por factores biológicos… porque algún cambio en los valores de grandes números impedirían la existencia del hombre para considerar el problema”.
93.000 millones de años luz
Dirac también intervino en esclarecer grandes problemas de la física.
Cuatro años más tarde desarrolló esta importante intuición con más detalle, con especial referencia a las coincidencias de los grandes números de Dirac, en una breve carta que se publicó en la revista Nature. Dicke argumentaba que formas de vidas bioquímicas como nosotros mismos deben su propia base química a elementos tales como el carbono, nitrógeno, el oxígeno y el fósforo que son sintetizados tras miles de millones de años de evolución estelar en la secuencia principal. (El argumento se aplica con la misma fuerza a cualquier forma de vida basada en cualesquiera elementos atómicos más pesados que el helio). Cuando las estrellas mueren, las explosiones que constituyen las supernovas dispersan estos elementos biológicos “pesados” por todo el espacio, de donde son incorporados en granos, planetesimales, planetas, moléculas “inteligentes” auto replicantes como ADN y, finalmente, en nosotros mismos que, en realidad, estamos hechos de polvo de estrellas.
Esta escala temporal está controlada por el hecho de que las constantes fundamentales de la naturaleza sean:
t(estrellas) ≈ (Gmp2 / hc)-1 h/mpc2 ≈ 1040 ×10-23 segundos ≈ 10.000 millones de años.
No esperaríamos estar observando el universo en tiempos significativamente mayores que t(estrellas), puesto que todas las estrellas estables se habrían expandido, enfriado y muerto. Tampoco seríamos capaces de ver el universo en tiempos mucho menores que t(estrellas) porque no podríamos existir; no había estrellas ni elementos pesados como el carbono. Parece que estamos amarrados por los hechos de la vida biológica para mirar el universo y desarrollar teorías cosmológicas una vez que haya transcurrido un tiempo t(estrellas) desde el Big Bang.
Así pues, el valor que del gran número nos dio Dirac N(t) no es en absoluto aleatorio. Debe tener un valor próximo al que toma N(t) cuando t esta cercano el valor t(estrella).
Todo lo que la coincidencia de Dirac dice es que vivimos en un tiempo de la Historia Cósmica posterior a la formación de las estrellas y anterior a su muerte. Esto no es sorprendente. Dicke nos está diciendo que no podríamos dejar de observar la coincidencia de Dirac: es un requisito para que exista vida como la nuestra
De esta forma Dicke nos vino a decir que:
“Para que el universo del Big Bang contenga las ladrillos básicos necesarios para la evolución posterior de la complejidad biológica-química debe tener una edad al menos tan larga, como el tiempo que se necesita para las reacciones nucleares en las estrellas produzcan esos elaborados elementos.”
Esto significa que el universo observable debe tener al menos diez mil millones de años y por ello, puesto que se está expandiendo, debe tener un tamaño de al menos diez mil millones de años luz. No podríamos existir en un universo que fuera significativamente más pequeño.
Un argumento hermosamente simple con respecto a la inevitabilidad del gran tamaño del universo para nosotros aparece por primera vez en el texto de las Conferencias Bampton impartidas por el teólogo de Oxford, Eric Mascall. Fueron publicadas en 1.956 y el autor atribuye la idea básica a Gerad Whitrow.
Estimulado por las sugerencias Whitrow, escribe:
“Si tenemos tendencia a sentirnos intimidados sólo por el tamaño del universo, está bien recordar que en algunas teorías cosmológicas existe una conexión directa entre la cantidad de materia en el universo y las condiciones en cualquier porción limitada del mismo, de modo que en efecto puede ser necesario que el universo tenga el enorme tamaño y la enorme complejidad que la astronomía moderna ha revelado para que la Tierra sea un posible hábitat para seres vivos.”
Esta simple observación puede ampliarse para ofrecernos una comprensión profunda de los sutiles lazos que existen entre aspectos superficialmente diferentes del universo que vemos a nuestro alrededor y las propiedades.
Claro que los procesos de la alquimia estelar necesitan tiempo: miles de millones de años de tiempo. Y debido a que nuestro universo se está expandiendo, tiene que tener un tamaño de miles de millones de años-luz para que durante ese periodo de tiempo necesario pudiera haber fabricado los componentes y elementos complejos para la vida. Un universo que fuera sólo del tamaño de nuestra Vía Láctea, con sus cien mil millones de estrellas resultaría insuficiente, su tamaño sería sólo de un mes de crecimiento-expansión y no habría producido esos elementos básicos para la vida.

El universo tiene la curiosa propiedad de hacer que los seres vivos piensen que sus inusuales propiedades son poco propicias para la vida, para la existencia de vida, cuando de hecho, es todo lo contrario; las propiedades del universo son esenciales para la vida. Lo que ocurre es que en el fondo tenemos miedo; nos sentimos muy pequeños ante la enorme extensión y tamaño del universo que nos acoge. Sabemos aún muy poco sobre sus misterios, nuestras capacidades son limitadas y al nivel de nuestra tecnología actual estamos soportando el peso de una gran ignorancia sobre muchas cuestiones que necesitamos conocer. Con sus miles de millones de galaxias y sus cientos de miles de millones de estrellas, si niveláramos todo el material del universo para conseguir un mar uniforme de materia, nos daríamos cuenta de lo poco que existe de cualquier cosa. La media de materia del universo está en aproximadamente 1 átomo por cada metro cúbico de espacio. Ningún laboratorio de la Tierra podría producir un vacío artificial que fuera remotamente parecido al vacio del espacio estelar. El vacío más perfecto que hoy podemos alcanzar en un laboratorio terrestre contiene aproximadamente mil millones de átomos por m3.

Esta nueva manera de mirar el universo nos da nuevas ideas, no todo el espacio son agujeros negros, estrellas de neutrones, galaxias y desconocidos planetas; la verdad es que casi todo el universo está vacío y sólo en algunas regiones tiene agrupaciones de materia en forma de estrellas y otros objetos estelares y cosmológicos; muchas de sus propiedades y características más sorprendentes (su inmenso tamaño y su enorme edad, la soledad y oscuridad del espacio) son condiciones necesarias para que existan observadores inteligentes como nosotros.



No debería sorprendernos la vida extraterrestre; si existe, pudiera ser tan rara y lejana para nosotros como en realidad nos ocurre aquí mismo en la Tierra, donde compartimos hábitat con otros seres vivos con los que hemos sido incapaces de comunicarnos, a pesar de que esas formas de vida, como la nuestra, están basadas también en el carbono. No se puede descartar formas de vida inteligente basadas en otros elementos, como por ejemplo, el silicio.
La baja densidad media de materia en el universo significa que si agregáramos material en estrellas o galaxias, deberíamos esperar que las distancias medias entre objetos fueran enormes.
El universo visible contiene sólo: 1 átomo por metro cúbico 1 Tierra por (10 años luz)3 1 Estrella por (103 años luz)3 1 Galaxia por (107 años luz)3 1 “Universo” por (1010 años luz)3
La consecuencia que de todo esto podemos obtener es que, el Universo (nuestro Universo), es como lo conocemos gracias a que las leyes que lo rigen son las que son y no otras diferentes. Las fuerzas fundamentales actúan sobre la materia presente, la materia se comporta siguiente el ritmo que el Universo les marca, las transformaciones se producen por el simple hecho de que todo lo que existe es dinámico, nada estático puede estar presente en nuestro Universo, y, ese movimiento o vibración, hace que las cosas cambien, se transformen y se eleven, es decir, a partir de sustancias o elementos simples, se convierten en complejos y, hasta tal punto es así que, esa complejidad llega hasta el máximo plano en el que la materia puede existir, ¡la vida! y, ésta, también tiene su propio ciclo de evolución que se traduce en la Conciencia, es decir, algunos seres vivos pueden llegar a alcanzar la consciencia a través de sus mentes y, siendo así, han podido alcanzar ese plano superior de entendimiento que reside en lo que llamamos Mente, lugar que es, en realidad, el que más conectado está con el Universo mismo del que, de alguna manera, forma parte.

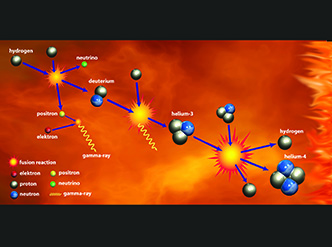

En el Universo se forjaron (los materiales que nos conforman y se hicieron en los núcleos estelares) y al Universo pertenecen, y, sin embargo, estamos en la fase de aprendizaje, aún no sabemos comunicarnos con ese Universo que nos trajo aquí, y, al que me gustaría preguntar: ¿Por qué nos has traído? ¿Qué función es la nuestra? ¿Qué destino nos tienes reservado?
¡Es todo tan complejo!
Pero, como decía Hilbert: “Tenemos que saber, sabremos”.
Emilio Silvera V.
Nov
23
Ya podemos “viajar” desde el núcleo atómico hasta las...
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Astronomía y Astrofísica ~
Clasificado en Astronomía y Astrofísica ~
 Comments (1)
Comments (1)
Interacciones fundamentales

Existen en el Universo cuatro fuerzas fundamentales (al menos son las que hasta el momento conocemos), éstas cuatro fuerzas son las que rigen en todas las regiones del Universo y, junto a las constantes universales, hacen que el Universo sea tal como lo podemos observar. Le dan un ritmo a los objetos que lo pueblan y, ya pueden estar conformados por “materia inerte” y tratarse de seres vivos, todo responde a sus mandatos y de acuerdo a ellos se comportan.
Nada de lo que sucede en el Universo es “porque sí”, todo tiene su por qué. Nos ha costado miles de años de pensamientos, de estudios, de observaciones, de experimentos y de experiencia el llegar a conocer, en cierta medida, como funciona la Naturaleza.

Siempre nos hemos equivocado pero… ¡Nos hemos vuelto a levantar!
En un Tiempo Pasado, algunos optimistas decían: “Ya nada nuevo podemos aprender, sabemos el origen y el por qué de todas las cosas” (La cita pertenece al filósofo francés del siglo XVII, Bernard Le Bovier de Fontenelle). Aquellos pobres ilusos, en realidad, eran unos grandes ignorantes que no eran conscientes de lo mucho que nos quedaba por saber. Las preguntas siguen siendo mucho más abundantes que las respuestas.
Un famoso Presidente de la Real Sociedad de Londres, ante todos los comensales dijo: “Nunca podremos saber de qué están hechas las estrellas.”

Y en el Presente lo sabemos perfectamente
También un famoso científico de su tiempo, ante un gran gentío dijo: Nunca nada más pesado que el aire podrá volar si no es un pájaro”.
fueron pronunciada por el científico Lord Kelvin, quien sostenía que las máquinas voladoras más pesadas que el aire eran imposibles.

Poco después remontó el vuelo el avión de los hermanos Wright.
Esto nos dice que debemos ser prudentes y no negar lo que pudiera ser en un futuro, porque hoy no tengamos los medios… ¡Mañana ya veremos!
El propio Rutherford empezó a vislumbrar la respuesta a la pregunta que arriba hacemos. Entre 1.906 y 1.908 (hace más de un siglo) realizó constantes experimentos disparando partículas alfa contra una lámina sutil de metal (como oro o platino), para analizar sus átomos. La mayor
que arriba hacemos. Entre 1.906 y 1.908 (hace más de un siglo) realizó constantes experimentos disparando partículas alfa contra una lámina sutil de metal (como oro o platino), para analizar sus átomos. La mayor parte de los proyectiles atravesaron la barrera sin desviarse (como balas a través de las hojas de un árbol), pero no todos.
parte de los proyectiles atravesaron la barrera sin desviarse (como balas a través de las hojas de un árbol), pero no todos.
En la placa fotográfica que le sirvió de blanco tras el metal, Rutherford descubrió varios impactos dispersos e insospechados alrededor del punto central. Comprobó que algunas partículas habían rebotado. Era como si en vez de atravesar las hojas, algunos proyectiles hubiesen chocado contra algo más sólido. Rutherford supuso que aquella “balas” habían chocado contra una especie de núcleo denso, que ocupaba sólo una parte mínima del volumen atómico y ese núcleo de intensa densidad desviaban los proyectiles que acertaban a chocar contra él. Ello ocurría en muy raras ocasiones, lo cual demostraba que los núcleos atómicos debían ser realmente ínfimos, porque un proyectil había de encontrar por fuerza muchos millones de átomos al atravesar la lámina metálica
por fuerza muchos millones de átomos al atravesar la lámina metálica
Era lógico suponer , pues, que los protones constituían ese núcleo duro. Rutherford representó los protones atómicos como elementos apiñados alrededor de un minúsculo “núcleo atómico” que servía de centro (después de todo eso, hemos podido saber
, pues, que los protones constituían ese núcleo duro. Rutherford representó los protones atómicos como elementos apiñados alrededor de un minúsculo “núcleo atómico” que servía de centro (después de todo eso, hemos podido saber que el diámetro de ese núcleo equivale a algo más de una cienmilésima del volumen total del átomo).
que el diámetro de ese núcleo equivale a algo más de una cienmilésima del volumen total del átomo).
En 1.908 se concedió a Rutherford el premio Nobel de Química por su extraordinaria labor de investigación sobre la naturaleza de la materia. Él fue el responsable de importantes descubrimientos que permitieron conocer la estructura de los átomos en esa primera avanzadilla.
de importantes descubrimientos que permitieron conocer la estructura de los átomos en esa primera avanzadilla.
Átomo de hidrógeno, núcleo y electrón.
Desde entonces se pueden describir con términos más concretos los átomos específicos y sus diversos comportamientos. Por ejemplo, el átomo de hidrógeno posee un solo electrón. Si se elimina, el protónrestante se asocia inmediatamente a alguna molécula vecina; y cuando el núcleo desnudo de hidrógeno no encuentra por este medio un electrón que participe, actúa como un protón (es decir, una partícula subatómica), lo cual le permite penetrar en la materia y reaccionar con otros núcleos si conserva la suficiente energía.
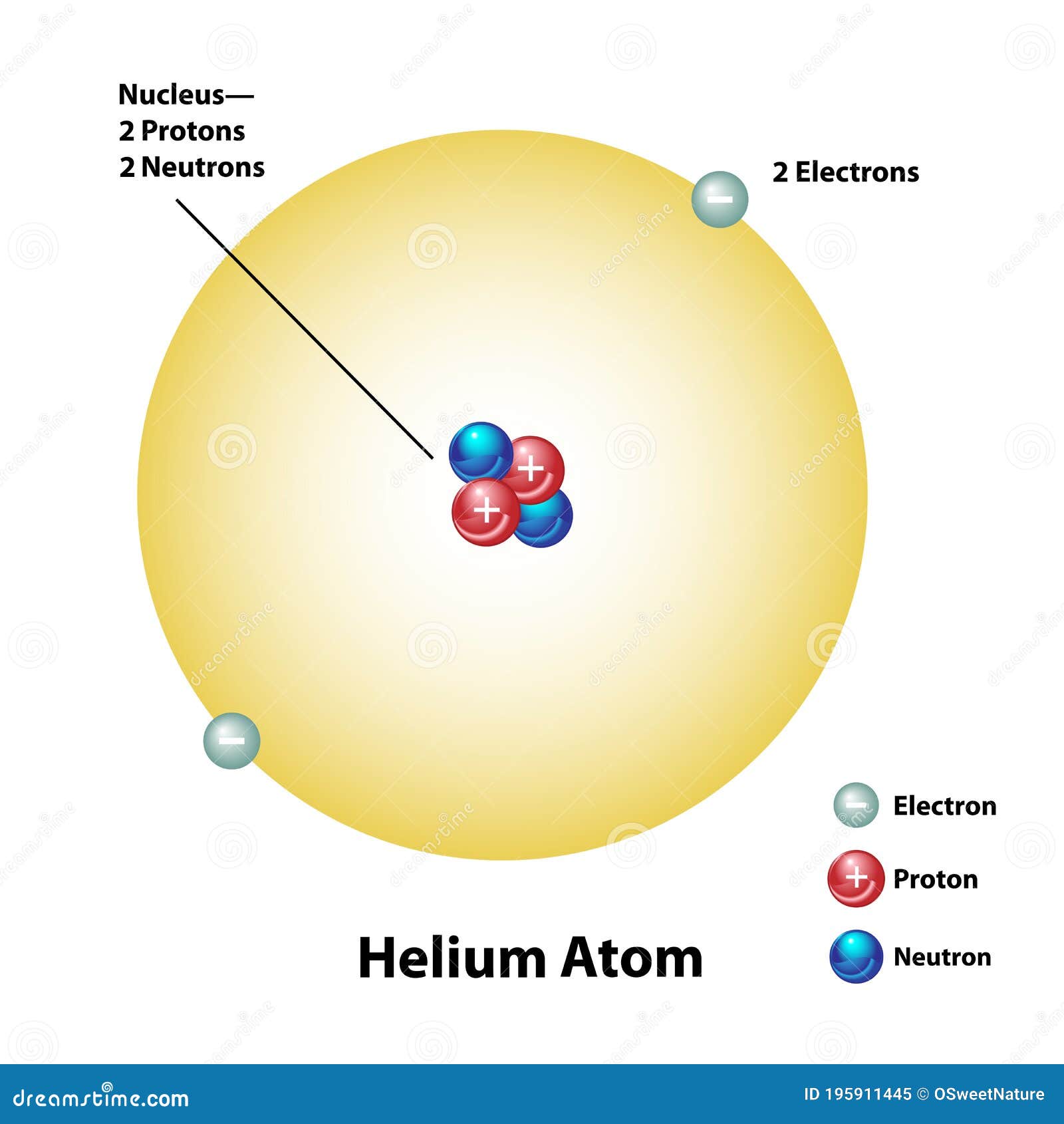
El helio, que posee dos electrones, no cede uno con tanta facilidad. Sus dos electrones forman un caparazón hermético, por lo cual el átomo es inerte. No obstante, si se despoja al helio de ambos electrones, se convierte en una partícula alfa, es decir
un caparazón hermético, por lo cual el átomo es inerte. No obstante, si se despoja al helio de ambos electrones, se convierte en una partícula alfa, es decir , una partícula subatómica portadora de dos unidades de carga positiva.
, una partícula subatómica portadora de dos unidades de carga positiva.
Hay un tercer elemento, el litio, cuyo átomo tiene tres electrones. Si se despoja de uno o dos, se transforma en ión, y si pierde los tres, queda reducida a un núcleo desnudo, con una carga positiva de tres unidades.
electrones. Si se despoja de uno o dos, se transforma en ión, y si pierde los tres, queda reducida a un núcleo desnudo, con una carga positiva de tres unidades.
Las unidades de carga positiva en el núcleo atómico deben ser numéricamente idénticas a los electrones que contiene por norma, pues el átomo suele ser un cuerpo neutro, y esta igualdad de lo positivo con lo negativo es el equilibrio. De hecho, los números atómicos de sus elementos se basan en sus unidades de carga positiva, no en las de carga negativa, porque resulta fácil hacer variar el número de electrones atómicos dentro de la formación
de electrones atómicos dentro de la formación iónica, pero en cambio se encuentran grandes dificultades si se desea alterar el número de sus protones.
iónica, pero en cambio se encuentran grandes dificultades si se desea alterar el número de sus protones.
Apenas esbozado este esquema de la construcción atómica, surgieron nuevos enigmas. El número de unidades con carga positiva en un núcleo no equilibró, en ningún caso, el peso nuclear ni la masa, exceptuando el caso del átomo de hidrógeno. Para citar un ejemplo, se averiguó que el núcleo de helio tenía una carga positiva dos veces mayor que la del núcleo de hidrógeno; pero como ya se sabía, su masa era cuatro veces mayor que la de este último. Y la situación empeoró progresivamente a medida que se descendía por la tabla de elementos, e incluso cuando se alcanzó el uranio, se encontró un núcleo con una masa igual a 238 protones, pero una carga que equivalía sólo a 92.
de unidades con carga positiva en un núcleo no equilibró, en ningún caso, el peso nuclear ni la masa, exceptuando el caso del átomo de hidrógeno. Para citar un ejemplo, se averiguó que el núcleo de helio tenía una carga positiva dos veces mayor que la del núcleo de hidrógeno; pero como ya se sabía, su masa era cuatro veces mayor que la de este último. Y la situación empeoró progresivamente a medida que se descendía por la tabla de elementos, e incluso cuando se alcanzó el uranio, se encontró un núcleo con una masa igual a 238 protones, pero una carga que equivalía sólo a 92.
¿Cómo era posible que un núcleo que contenía cuatro protones (según se suponía el núcleo de helio) tuviera sólo dos unidades de carga positiva? Según la más simple y primera conjetura emitida, la presencia en el núcleo de partículas cargadas negativamente y con peso despreciable neutralizaba dos unidades de carga. Como es natural, se pensó también en el electrón. Se podría componer el rompecabezas si se suponía que en núcleo de helio estaba integrado por cuatro protones y dos electronesneutralizadores, lo cual deja libre una carga positiva neta de dos, y así sucesivamente, hasta llegar al uranio, cuyo núcleo tendría, pues, 238 protones y 146 electrones, con 92 unidades libres de carga positiva. El hecho de que los núcleos radiactivos emitieran electrones (según se había comprobado ya, por ejemplo, en el caso de las partículas beta), reforzó esta idea general
y primera conjetura emitida, la presencia en el núcleo de partículas cargadas negativamente y con peso despreciable neutralizaba dos unidades de carga. Como es natural, se pensó también en el electrón. Se podría componer el rompecabezas si se suponía que en núcleo de helio estaba integrado por cuatro protones y dos electronesneutralizadores, lo cual deja libre una carga positiva neta de dos, y así sucesivamente, hasta llegar al uranio, cuyo núcleo tendría, pues, 238 protones y 146 electrones, con 92 unidades libres de carga positiva. El hecho de que los núcleos radiactivos emitieran electrones (según se había comprobado ya, por ejemplo, en el caso de las partículas beta), reforzó esta idea general . Dicha teoría prevaleció durante más de una década, hasta que por caminos indirectos, llegó una respuesta mejor como resultado de otras investigaciones.
. Dicha teoría prevaleció durante más de una década, hasta que por caminos indirectos, llegó una respuesta mejor como resultado de otras investigaciones.
Pero entre tanto se habían presentado algunas objeciones rigurosas contra dicha hipótesis. Por lo pronto , si el núcleo estaba constituido esencialmente de protones, mientras que los ligeros electrones no aportaban prácticamente ninguna contribución a la masa, ¿Cómo se explicaba que las masas relativas de varios núcleos no estuvieran representadas por número
, si el núcleo estaba constituido esencialmente de protones, mientras que los ligeros electrones no aportaban prácticamente ninguna contribución a la masa, ¿Cómo se explicaba que las masas relativas de varios núcleos no estuvieran representadas por número enteros? Según los pesos atómicos conocidos, el núcleo del átomo cloro, por ejemplo, tenía una masa 35’5 veces mayor que la del núcleo de hidrógeno. ¿Acaso significaba esto que contenía 35’5 protones? Ningún científico (ni entonces ni ahora) podía aceptar la existencia de medio protón.
enteros? Según los pesos atómicos conocidos, el núcleo del átomo cloro, por ejemplo, tenía una masa 35’5 veces mayor que la del núcleo de hidrógeno. ¿Acaso significaba esto que contenía 35’5 protones? Ningún científico (ni entonces ni ahora) podía aceptar la existencia de medio protón.
Este singular interrogante encontró una respuesta incluso antes de solventar el problema principal , y ello dio lugar a una interesante historia.
, y ello dio lugar a una interesante historia.

Los tres isótopos naturales del carbono: carbono-12 (6 protones y 6 neutrones), carbono-13 (6 protones y 7 neutrones) y carbono-14 (6 protones y 8 neutrones). En los tres casos es carbono, tiene el aspecto de carbono y se comporta químicamente como carbono, por tener seis protones (y forma parte de nuestro organismo, por ejemplo). Sin embargo, sus propiedades físicas varían. Por ejemplo, mientras que el carbono-12 y el carbono-13 son estables, el carbono-14 es inestable y radioactivo: emite radiación beta, uno de sus neutrones “extras” se transforma así en un protón y el núcleo se convierte en nitrógeno-14 (que tiene 7 protones y 7 neutrones), con el aspecto y las propiedades del nitrógeno (por tener 7 protones). Dado que la mitad de la masa del carbono-14 pasa a ser nitrógeno-14 cada 5.730 años aproximadamente (más o menos lo que llevamos de civilización humana), la presencia de este isótopo natural resulta especialmente útil para la datación precisa de objetos históricos.
Isótopos; construcción de bloques uniformes
Allá por 1.816, el físico inglés William Prout había insinuado ya que el átomo de hidrógeno debía entrar  en la constitución de todos los átomos. Con el tiempo se fueron desvelando los pesos atómicos, y la teoría de Prout quedó arrinconada, pues se comprobó que muchos elementos tenían pesos fraccionarios (para lo cual se tomó el oxígeno, tipificado al 16). El cloro, según dije antes, tiene un peso atómico aproximado de 35’5, o para ser exactos, 35’457. otros ejemplos son el antimonio, con un peso atómico de 121’75, el galio con 137’34, el boro con 10’811 y el cadmio con 112’40.
en la constitución de todos los átomos. Con el tiempo se fueron desvelando los pesos atómicos, y la teoría de Prout quedó arrinconada, pues se comprobó que muchos elementos tenían pesos fraccionarios (para lo cual se tomó el oxígeno, tipificado al 16). El cloro, según dije antes, tiene un peso atómico aproximado de 35’5, o para ser exactos, 35’457. otros ejemplos son el antimonio, con un peso atómico de 121’75, el galio con 137’34, el boro con 10’811 y el cadmio con 112’40.

El Uranio 235 que es el único que de manera natural es apto para la fisión nuclear, es escaso, sólo el 7 por 1.000 es uranio 235, el resto , es uranio 238 que, no es combustible nuclear y, como la madera mojada, no arde. Sin embargo, si se bombardea con neutrones lentos del uranio 235, resulta que se convierte en Plutonio 239 que sí, es combustible nuclear válido. ¡Qué no idearemos para conseguir
, es uranio 238 que, no es combustible nuclear y, como la madera mojada, no arde. Sin embargo, si se bombardea con neutrones lentos del uranio 235, resulta que se convierte en Plutonio 239 que sí, es combustible nuclear válido. ¡Qué no idearemos para conseguir los objetivos!
los objetivos!
El Uranio es muy radiactivo y si está enriquecido… ¡Ya sabemos las consecuencias!
Hacia principios de siglo se hizo una serie de observaciones desconcertantes, que condujeron al esclarecimiento. El inglés William Crookes (el del tubo Crookes) logró disociar del uranio una sustancia cuya ínfima cantidad resultó ser mucho más radiactiva que el propio uranio. Apoyándose en su experimento, afirmó que el uranio no tenía radiactividad, y que ésta procedía exclusivamente de dicha impureza, que él denominó uranio X. Por otra parte, Henri Becquerel descubrió que el uranio purificado y ligeramente radiactivo adquiría mayor radiactividad con el tiempo, por causas desconocidas. Si se deja reposar durante algún tiempo, se podía
de observaciones desconcertantes, que condujeron al esclarecimiento. El inglés William Crookes (el del tubo Crookes) logró disociar del uranio una sustancia cuya ínfima cantidad resultó ser mucho más radiactiva que el propio uranio. Apoyándose en su experimento, afirmó que el uranio no tenía radiactividad, y que ésta procedía exclusivamente de dicha impureza, que él denominó uranio X. Por otra parte, Henri Becquerel descubrió que el uranio purificado y ligeramente radiactivo adquiría mayor radiactividad con el tiempo, por causas desconocidas. Si se deja reposar durante algún tiempo, se podía extraer de él repetidas veces uranio activo X. Para decirlo de otra manera, por su propia radiactividad, el uranio se convertía en el uranio X, más radiactivo aún.
extraer de él repetidas veces uranio activo X. Para decirlo de otra manera, por su propia radiactividad, el uranio se convertía en el uranio X, más radiactivo aún.
Por entonces, Rutherford, a su vez, separó del torio un torio X muy radiactivo, y comprobó también que el torio seguía produciendo más torio X. Hacia aquellas fechas se sabía ya que el más famoso de los elementos radiactivos, el radio , emitía un gas radiactivo, denominado radón. Por tanto, Rutherford y su ayudante, el químico Frederick Soddy, dedujeron que durante la emisión de sus partículas los átomos radiactivos se transformaron en otras variedades de átomos radiactivos.
, emitía un gas radiactivo, denominado radón. Por tanto, Rutherford y su ayudante, el químico Frederick Soddy, dedujeron que durante la emisión de sus partículas los átomos radiactivos se transformaron en otras variedades de átomos radiactivos.
El Radón, uno de los llamados gases nobles, es incoloro, inodoro e insípido, además de –para nuestro mal- radioactivo. Suele presentarse según el tipo de suelos de determinadas zonas y con la descomposición de uranio, concentrándose en la superficie y siendo “arrastrado” en y por el aire que respiramos, y es en grandes cantidades es un gas perjudicial para la salud… y que anticipa terremotos.
Varios químicos que investigaron tales transformaciones lograron obtener un surtido muy variado de nuevas sustancias, a las que dieron nombres tales como radio
químicos que investigaron tales transformaciones lograron obtener un surtido muy variado de nuevas sustancias, a las que dieron nombres tales como radio A, radio
A, radio B, mesotorio I, mesotorio II y actinio C. Luego los agruparon todos en tres series, de acuerdo con sus historiales atómicos. Una serie se originó del uranio disociado; otra del torio, y la tercera del actinio (si bien más tarde se encontró un predecesor del actinio, llamado protactinio).
B, mesotorio I, mesotorio II y actinio C. Luego los agruparon todos en tres series, de acuerdo con sus historiales atómicos. Una serie se originó del uranio disociado; otra del torio, y la tercera del actinio (si bien más tarde se encontró un predecesor del actinio, llamado protactinio).
En total se identificaron unos cuarenta miembros de esas series, y cada uno se distinguió por su peculiar esquema de radiación. Pero los productos finales de las tres series fueron idénticos: en último término, todas las cadenas de sustancias conducían al mismo elemento, el plomo.
finales de las tres series fueron idénticos: en último término, todas las cadenas de sustancias conducían al mismo elemento, el plomo.
Ahora bien, esas cuarenta sustancias no podían ser, sin excepción, elementos disociados. Entre el uranio (92) y el plomo (82) había sólo diez lugares en la tabla periódica, y todos ellos, salvo dos, pertenecían a elementos conocidos.
En realidad, los químicos descubrieron que aunque las sustancias diferían entre sí por su radiactividad, algunas tenían propiedades químicas idénticas. Por ejemplo, ya en 1.907 los químicos americanos Herbert Newby McCoy y W. H. Ross descubrieron que el radio-torio (uno entre los varios productos de la desintegración del torio) mostraba el mismo comportamiento químico que el torio, y el radio
de la desintegración del torio) mostraba el mismo comportamiento químico que el torio, y el radio D, el mismo que el plomo, tanto que a veces era llamado radio-plomo. De todo lo cual se infirió que tales sustancias eran en realidad variedades de mismo elemento: el radio-torio, una forma de torio; el radio-plomo, un miembro de una familia de plomos; y así sucesivamente.
D, el mismo que el plomo, tanto que a veces era llamado radio-plomo. De todo lo cual se infirió que tales sustancias eran en realidad variedades de mismo elemento: el radio-torio, una forma de torio; el radio-plomo, un miembro de una familia de plomos; y así sucesivamente.
En 1.913, Soddy esclareció esta idea y le dio más amplitud. Demostró que cuando un átomo emitía una partícula alfa, se transformaba en un elemento que ocupaba dos lugares más abajo en la lista de elementos, y que cuando emitía una partícula beta, ocupaba, después de su transformación, el lugar inmediatamente superior . Con arreglo a tal norma, el radiotorio descendía en la tabla hasta el lugar del torio, y lo mismo ocurría con las sustancias denominadas uranio X y uranio Y, es decir, que los tres serían variedades del elemento 90. Así mismo, el radio D, el radio B, el torio B y el actinio B compartirían el lugar del plomo como variedades del elemento 82.
. Con arreglo a tal norma, el radiotorio descendía en la tabla hasta el lugar del torio, y lo mismo ocurría con las sustancias denominadas uranio X y uranio Y, es decir, que los tres serían variedades del elemento 90. Así mismo, el radio D, el radio B, el torio B y el actinio B compartirían el lugar del plomo como variedades del elemento 82.
Soddy dio el nombre de isótopos (del griego iso y topos, “el mismo lugar”) a todos los miembros de una familia de sustancias que ocupaban el mismo lugar en la tabla periódica. En 1.921 se le concedió el premio Nobel de Química.
de isótopos (del griego iso y topos, “el mismo lugar”) a todos los miembros de una familia de sustancias que ocupaban el mismo lugar en la tabla periódica. En 1.921 se le concedió el premio Nobel de Química.
El modelo protón–electrón del núcleo concordó perfectamente con la teoría de Soddy sobre los isótopos. Al retirar una partícula alfa de un núcleo, se reducía en dos unidades la carga positiva de dicho núcleo, exactamente lo que necesitaba para bajar dos lugares en la tabla periódica. Por otra parte, cuando el núcleo expulsaba un electrón (partícula beta), quedaba sin neutralizar un protón adicional, y ello incrementaba en una unidad la carga positiva del núcleo, lo cual era como agregar una unidad al número atómico, y por tanto, el elemento pasaba a ocupar la posición inmediatamente superior en la tabla periódica de los elementos. ¡Maravilloso!
atómico, y por tanto, el elemento pasaba a ocupar la posición inmediatamente superior en la tabla periódica de los elementos. ¡Maravilloso!
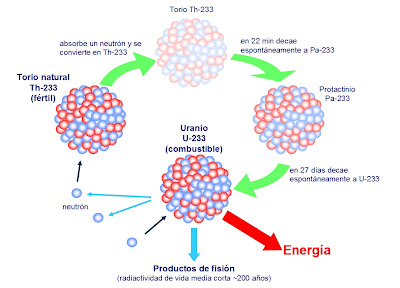
¿Cómo se explica que cuando el torio se descompone en radio-torio después de sufrir no una, sino tres desintegraciones, el producto siga siendo torio? Pues bien, en este proceso el átomo de torio pierde una partícula alfa, luego una partícula beta, y más tarde una segunda partícula beta. Si aceptamos la teoría sobre el bloque constitutivo de los protones, ello significa que el átomo ha perdido cuatro electrones (dos de ellos contenidos presuntamente en la partícula alfa) y cuatro protones. (La situación actual difiere bastante de este cuadro , aunque en cierto modo, esto no afecta al resultado).
, aunque en cierto modo, esto no afecta al resultado).
El núcleo de torio constaba inicialmente (según se suponía) de 232 protones y 142 electrones. Al haber perdido cuatro protones y otros cuatro electrones, quedaba reducido a 228 protones y 138 electrones. No obstante, conservaba todavía el número atómico 90, es decir, el mismo de antes.
atómico 90, es decir, el mismo de antes.
Así pues, el radiotorio, a semejanza del torio, posee 90 electrones planetarios, que giran alrededor del núcleo. Puesto que las propiedades químicas de un átomo están sujetas al número de sus electrones planetarios, el torio y el radiotorio tienen el mismo comportamiento químico, sea cual fuere su diferencia en peso atómico (232 y 228 respectivamente).
de sus electrones planetarios, el torio y el radiotorio tienen el mismo comportamiento químico, sea cual fuere su diferencia en peso atómico (232 y 228 respectivamente).
Los isótopos de un elemento se identifican por su peso atómico, o número másico. Así, el torio corriente se denomina torio 232, y el radio-torio, torio 228. Los isótopos radiactivos del plomo se distinguen también por estas denominaciones: plomo 210 (radio D), plomo 214 (radio B), plomo 212 (torio B) y plomo 211 (actinio B).
Se descubrió que la noción de isótopo podía aplicarse indistintamente tanto a los elementos estables como a los radiactivos. Por ejemplo, se comprobó que las tres series radiactivas anteriormente mencionadas terminaban en tres formas distintas de plomo. La serie del uranio acababa en plomo 206, la del torio en plomo 208 y la del actinio en plomo 207. cada uno de estos era un isótopo estable y corriente del plomo, pero los tres plomos diferían por su peso atómico.
Mediante un dispositivo inventado por cierto ayudante de J. J. Thomson, llamado Francis William Aston, se demostró la existencia de los isótopos estables. En 1.919, Thomson, empleando la versión primitiva de aquel artilugio, demostró que el neón estaba constituido por dos variedades de átomos: una cuyo número de masa era 20, y otra con 22. El neón 20 era el isótopo común; el neón 22 lo acompañaba en la proporción de un átomo cada diez. Más tarde se descubrió un tercer isótopo, el neón 21, cuyo porcentaje en el neón atmosférico era de un átomo por cada 400.
de masa era 20, y otra con 22. El neón 20 era el isótopo común; el neón 22 lo acompañaba en la proporción de un átomo cada diez. Más tarde se descubrió un tercer isótopo, el neón 21, cuyo porcentaje en el neón atmosférico era de un átomo por cada 400.
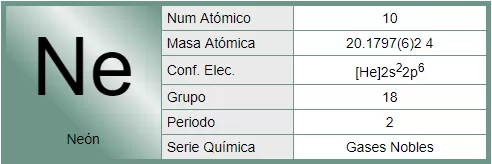
Entonces fue posible, al fin, razonar el peso atómico fraccionario de los elementos. El peso atómico del neón (20, 183) representaba el peso conjunto de los tres isótopos, de pesos diferentes, que integraban el elemento en su estado natural. Cada átomo individual tenía un número másico entero, pero el promedio de sus masas (el peso atómico) era un número fraccionario.
másico entero, pero el promedio de sus masas (el peso atómico) era un número fraccionario.
Aston procedió a mostrar que varios elementos estables comunes eran, en realidad, mezclas de isótopos. Descubrió que el cloro, con un peso atómico fraccionario de 35’453, estaba constituido por el cloro 35 y el cloro 37, en la proporción de cuatro a uno. En 1.922 se le otorgó el premio Nobel de Química.
que varios elementos estables comunes eran, en realidad, mezclas de isótopos. Descubrió que el cloro, con un peso atómico fraccionario de 35’453, estaba constituido por el cloro 35 y el cloro 37, en la proporción de cuatro a uno. En 1.922 se le otorgó el premio Nobel de Química.
Sabiendo todo lo anteriormente explicado, hemos llegado a comprender cómo parte de la Astronomía que estudia las características físicas y químicas de los cuerpos celestes, la astrofísica es la parte más importante de la astronomía en la actualidad debido a que, al avanzar la física moderna: Efecto Doppler-Fizeau, el efecto Zeeman, las teorías cuánticas y las reacciones termonucleares aplicadas al estudio de los cuerpos celestes han permitido descubrir que el campo
de la astronomía en la actualidad debido a que, al avanzar la física moderna: Efecto Doppler-Fizeau, el efecto Zeeman, las teorías cuánticas y las reacciones termonucleares aplicadas al estudio de los cuerpos celestes han permitido descubrir que el campo magnético solar, el estudio de las radiaciones estelares y sus procesos de fusión nuclear, y determinar la velocidad radial de las estrellas, etc. La radiación electromagnética de los cuerpos celestes permite realizar análisis de los espectros que nos dicen de qué están hechas las estrellas y los demás cuerpos del espacio interestelar y, de esa manera, hemos ido conociendo la materia y sus secretos que cada vez, van siendo menos.
magnético solar, el estudio de las radiaciones estelares y sus procesos de fusión nuclear, y determinar la velocidad radial de las estrellas, etc. La radiación electromagnética de los cuerpos celestes permite realizar análisis de los espectros que nos dicen de qué están hechas las estrellas y los demás cuerpos del espacio interestelar y, de esa manera, hemos ido conociendo la materia y sus secretos que cada vez, van siendo menos.
Emilio Silvera V.
Nov
23
Imaginamos misiones que están fuera de nuestro alcance
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en General ~
Clasificado en General ~
 Comments (0)
Comments (0)
Por algunos de los trabajos aquí publicados, los viitn5tes asiduos conocen mi fascinación por ese “Mundo” llamado PANDORA, que nos han mostrado en la película AVATAR. Es fascinante la simbiosis que existe entre los habitantes de Pandora y el mismo planeta, en una relación mental extrema de comunicación mutua.
En fin amigos, cada cual que saque sus propias conclusiones.
Nov
22
Si la Tierra bosteza… ¡Nosotros a temblar!
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en General ~
Clasificado en General ~
 Comments (0)
Comments (0)
Vivimos en un planeta que está vivo, es dinámico y se recicla continuamente. Alguien llamó a la Tierra GAIA, es decir, un Ser viviente. El nombre “Gaia” para la Tierra proviene de la mitología griega, donde Gaia (o Gea) es la diosa de la Madre Tierra. El término griego Gaia (γαῖα) significa literalmente “Tierra o suelo” y es el origen de palabras como geología y geografía.
Como tantas veces he reseñado en este lugar, nosotros estamos a merced del planeta, no tenemos los medios para evitar sus “actividades” cotidianas de Tectónica de placas, erupciones volcánicas, terremotos, Tsunamis, Huracanes y Tornados…
Todo está cambiando ante nuestros ojos y somos testigos de lo inevitable. El inexorable transcurrir del Tiempo lo cambia todo y, nuestro mundo, no es una excepción.
Llegará el momento (si es que aún seguimos por aquí), en el que, la Humanidad tenga que buscar otro lugar, otros mundos para dar el primer paso a un nuevo comienzo. Acordaos de la Edad del Hielo y de otras eras geológicas en las que, difícilmente, podríamos vivir.
Espero que para cuando eso tenga lugar, hayamos podido conseguir tecnologías y medios que nos posibiliten la escapada de este querido mundo. Claro que, si para entonces no hemos sido los causantes de nuestra propia destrucción.
Dela Humanidad lo podemos esperar todo: Lo mejor y también lo peor.
Emilio Silvera V.
















 Totales: 82.785.839
Totales: 82.785.839 Conectados: 36
Conectados: 36