Ago
12
Moléculas, sustancias, cuerpos…
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Física-química ~
Clasificado en Física-química ~
 Comments (0)
Comments (0)
Es allí, en las estrellas, en sus hornos nucleares y en las explosiones de supernovas, donde a miles de millones de grados de temperatura, se crean los elementos más complejos que el hidrógeno y el helio. Aparece el litio, el carbono, el silicio o el nitrógeno y el hierro.

De estos materiales estamos nosotros hechos, y, lógicamente, se fabricaron en las estrellas.
En una supernova, en orden decreciente tenemos la secuencia de núcleos H, He, O, C, N, Fe, que coincide bastante bien con una ordenación en la tabla periódica que es:
H, He, (Li, Be, B) C, N, O…… Fe
¿Apreciáis la maravilla? Las estrellas brillan en el cielo para hacer posible que nosotros estemos aquí descubriendo los enigmas del Universo y…. de la vida inteligente.

El telescopio VLT (Very Large Telescope) de ESO ha obtenido imágenes de una fascinante región de formación de estrellas en la Gran Nube de Magallanes — una de las galaxias satélite de la Vía Láctea. Esta precisa imagen revela dos peculiares y brillantes nubes de gas: la rojiza NGC 2014 y su vecina azulada NGC 2020. Pese a que son muy diferentes, ambas fueron esculpidas por potentes vientos estelares procedentes de estrellas recién nacidas extremadamente calientes que también irradian el gas, provocando que brille de forma intensa. (para verla entera hay que pasar la rgla hacia la derehca).
Pero está claro que, todo el proceso estelar evolutivo inorgánico nos condujo desde el simple gas y polvo cósmico a la formación de estrellas y nebulosas solares hasta los planetas, la Tierra en particular, en cuyo medio ígneo describimos la formación de las estructuras de los silicatos, desplegándose con ello una enorme diversidad de composiciones, formas y colores, asistiéndose, por primera vez en la historia de la materia, a unas manifestaciones que contrastan con las que hemos mencionado en relación al proceso de las estrellas.
Desde el punto de vista del orden es la primera vez que nos encontramos con objetos de tamaño comparables al nuestro, en los que la ordenación de sus constituyentes es el rasgo más característico.
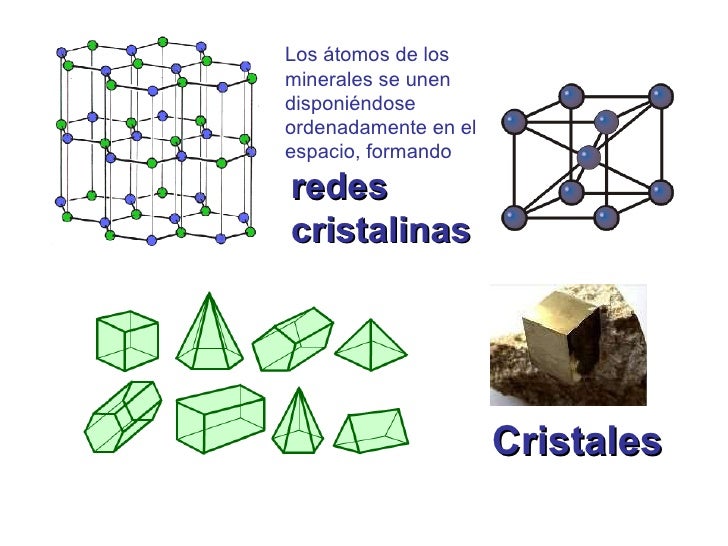
Al mismo tiempo nos ha parecido reconocer que esos objetos, es decir, sus redes cristalinas “reales”, almacenan información (memoria) que se nos muestra muy diversa y que puede cobrar interés en ciertos casos, como el de los microcristales de arcilla, en los que, según Cairos-Swith, puede incluso llegar a transmitirse.
Porque ¿qué sabemos en realidad de lo que llamamos materia inerte? Lo único que sabemos de ella son los datos referidos a sus condiciones físicas de dureza, composición, etc., en otros aspectos, ni sabemos si pueden existir otras propiedades distintas a las meramente-físicas.
¿No os hace pensar que nosotros estemos hechos, precisamente, de lo que llamamos materia inerte?

Pero el mundo inorgánico es sólo una parte del inmenso mundo molecular. El resto lo constituye el mundo orgánico, que es el de las moléculas que contienen carbono y otros átomos y del que quedan excluidos, por convenio y características especiales, los carbonatos, bicarbonatos y carburos metálicos, los cuales se incluyen en el mundo inorgánico.
Según decía en páginas anteriores, los quarks u y d se hallan en el seno de los nucleones (protones y neutrones) y, por tanto, en los núcleos atómicos. Hoy día, estos se consideran como una subclase de los hadrones.
La composición de los núcleos (lo que en Química se llama análisis cualitativo) es extraordinariamente sencilla ya que, como es sabido, constan de neutrones y protones que se pueden considerar como unidades que, dentro del núcleo, mantienen su identidad. Tal simplicidad cualitativa recuerda, por ejemplo, el caso de las series orgánicas, siendo la de los hidrocarburos saturados la más conocida. Recordad que su fórmula general es , lo que significa que una molécula de hidrocarburo contiene n átomos de carbono (símbolo C) y (2n+2) átomos de hidrógeno (símbolo H).
Protones y de neutrones determinan el elemento
El número de protones y neutrones determina al elemento, desde el hidrógeno (el más simple), al Uranio (el más complejo), siempre referido a elementos naturales que son 92, el resto, son artificiales, los conocidos transuránicos en cuyo grupo están el Einstenio o el Plutonio, artificiales todos ellos.
Los núcleos, como sistemas dinámicos de nucleones, pertenecen obviamente a la microfísica y, por consiguiente, para su descripción es necesario acudir a la mecánica cuántica. La materia, en general, aunque presumimos de conocerla, en realidad, nos queda mucho por aprender de ella.
Hablemos un poco de moléculas.

El papel primordial del agua en el metabolismo de los seres vivos se debe sus propiedades físicas y químicas, derivadas de la estructura molecular.
El número de especimenes atómicos es finito, existiendo ciertas razones para suponer que hacia el número atómico 173 los correspondientes núcleos serían inestables, no por razones intrínsecas de inestabilidad “radiactiva” nuclear, sino por razones relativistas. Ya antes me referiría a las especies atómicas, naturales y artificiales que son de unos pocos millares; en cambio; el número de moléculas conocidas hasta ahora comprende varios millones de especimenes, aumentando continuamente el número de ellas gracias a las síntesis que se llevan a cabo en numerosos laboratorios repartidos por todo el mundo.
Una molécula es una estructura, con individualidad propia, constituida por núcleos y electrones. Obviamente, en una molécula las interacciones deben tener lugar entre núcleos y electrones, núcleos y núcleos y electrones y electrones, siendo del tipo electromagnético.

Proteina supresora de tumores p53 encajada a una secuencia de ADN
Debido al confinamiento de los núcleos, el papel que desempeñan, aparte del de proporcionar la casi totalidad de la masa de la molécula, es poco relevante, a no ser que se trate de moléculas livianas, como la del hidrógeno. De una manera gráfica podríamos decir que los núcleos en una molécula constituyen el armazón de la misma, el esqueleto, cuya misión sería proporcionar el soporte del edificio. El papel más relevante lo proporcionan los electrones y en particular los llamados de valencia, que son los que de modo mayoritario intervienen en los enlaces, debido a que su energía es comparativamente inferior a la de los demás, lo que desempeña muy importante papel en la evolución.

Desde las moléculas más sencilla, como la del hidrógeno, con un total de 2 electrones, hasta las más complejas, como las de las proteínas, con muchos miles de ellos, existe toda una gama, según decía, de varios millones. Esta extraordinaria variedad de especies moleculares contrasta con la de las especies nucleares e incluso atómicas.
Sin entrar en las posibles diferencias interpretativas de estas notables divergencias, señalaré que, desde el punto de vista de la información, las especies moleculares la poseen en mucho mayor grado que los nucleares y atómicas.
Dejando aparte los núcleos, la información que soportan los átomos se podría atribuir a la distribución de su carga eléctrica, y en particular a la de los electrones más débilmente ligados. Concretando un poco se podría admitir que la citada información la soportan los orbitales atómicos, pues son precisamente estos orbitales las que introducen diferencias “geométricas” entre los diferentes electrones corticales.
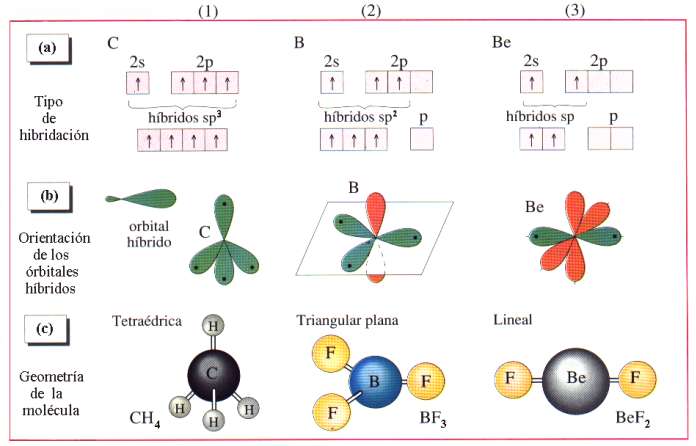
Justamente esa información es la que va a determinar las capacidades de unión de unos átomos con otros, previo el “reconocimiento” entre los orbitales correspondientes. De acuerdo con la mecánica cuántica el número de orbitales se reduce a unos pocos. Se individualizan por unas letras hablándose de orbitales, s, p, d, f, g, h. Este pequeño número nos proporciona una gran diversidad.
La llamada hibridación (una especie de mezcla) de orbitales es un modo de aumentar el número de mensajes, esto es, la información, bien entendido que esta hibridación ocurre en tanto y en cuanto dos átomos se preparan para enlazarse y formar una molécula. En las moléculas, la información, obviamente, debe de abarcar a todo el edificio, por lo que en principio parece que debería ser más rica que en los átomos. La ganancia de información equivale a una disminución de entropía; por esta razón, a la información se la llama también negantropía.
En términos electrónicos, la información se podría considerar proporcionada por un campo de densidad eléctrica, con valles, cimas, collados, etc., es decir, curvas isoelectrónicas, equivalentes formalmente a las de nivel en topografía. Parece razonable suponer que cuanto más diverso sean los átomos de una molécula, más rica y variada podrá ser su información, la información que pueda soportar.
La enorme variedad de formas, colores, comportamientos, etc., que acompaña a los objetos, incluidos los vivientes, sería una consecuencia de la riqueza en la información que soportan las moléculas (y sus agregados) que forman parte de dichos objetos. Ello explicaría que las moléculas de la vida sean en general de grandes dimensiones (macromoléculas). La inmensa mayoría de ellas contiene carbono. Debido a su tetravalencia y a la gran capacidad que posee dicho átomo para unirse consigo mismo, dichas moléculas pueden considerarse como un esqueleto formado por cadenas de esos átomos.
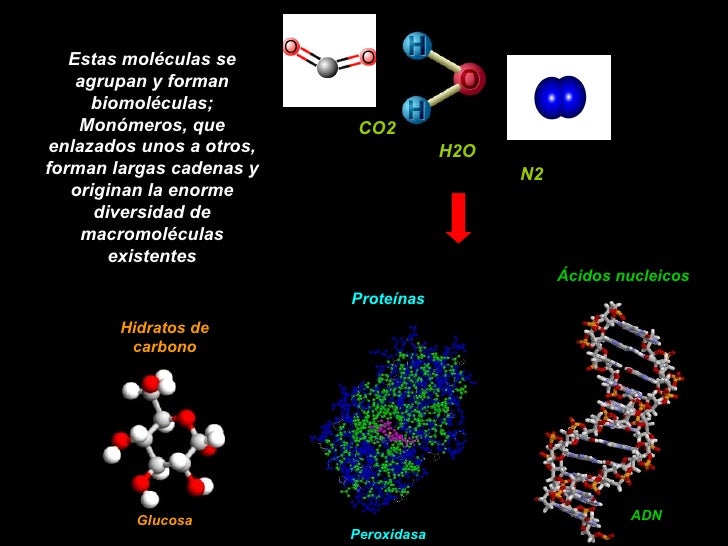
Estas moléculas se agrupan y forman biomoléculas; Monómeros, que enlazados unos a otros, forman largas cadenas y originan la enorme diversidad de macromoléculas existentes CO2 H2O N2 Hidratos de carbono Glucosa Peroxidasa.
El carbono no es el único átomo con capacidad para formar los citados esqueletos. Próximos al carbono en la tabla periódica, el silicio, fósforo y boro comparten con dicho átomo esa característica, si bien en un grado mucho menor.
Refiriéndonos al silicio, que para nosotros es el más importante, señalaremos que las “moléculas” que dicho átomo forma con el oxígeno y otros átomos, generalmente metálicos, poseyendo gran nivel de información, difieren, en varios aspectos, de las moléculas orgánicas, es decir, de las que poseen un esqueleto de átomos de carbono.

El mundo de los silicatos es de una gran diversidad, existiendo centenares de especies minerológicas. Esas diferencias se refieren, fundamentalmente, a que el enlace químico en el caso de las moléculas orgánicas es covalente, y cuando se forma la sustancia correspondiente (cuatrillones de moléculas) o es un líquido, como es el caso de los aceites, o bien un sólido que funde fácilmente. Entre las moléculas que lo forman se ejercen unas fuerzas, llamadas de van der Waals, que, pueden considerarse como residuales de las fuerzas electromagnéticas, algo más débiles que éstas. En cambio, en los silicatos sólidos (como en el caso del topacio) el enlace covalente o iónico no se limita a una molécula, sino que se extiende en el espacio ocupado por el sólido, resultando un entramado particularmente fuerte.
Al igual que para los cristales de hielo, en la mayoría de los silicatos la información que soportan es pequeña, aunque conviene matizar este punto. Para un cristal ideal así sería en efecto, pero ocurre que en la realidad el cristal ideal es una abstracción, ya que en el cristal real existen aquí y allá los llamados defectos puntuales que trastocan la periodicidad espacial propia de las redes ideales. Precisamente esos defectos puntuales podían proporcionar una mayor información.

Las moléculas orgánicas con enlaces dobles ó triples tienen también formas características.
Si prescindimos de las orgánicas, el resto de las moléculas que resultan de la combinación entre los diferentes átomos no llega a 100.000, frente a los varios millones de las primeras. Resulta ranozable suponer que toda la enorme variedad de moléculas existentes, principalmente en los planetas rocosos, se haya formado por evolución de los átomos, como corresponde a un proceso evolutivo. La molécula poseería mayor orden que los átomos de donde procede, esto es, menor entropía. En su formación, el ambiente se habría desordenado al ganar entropía en una cierta cantidad tal, que arrojarse un balance total positivo.
No puedo, dejar pasar la oportunidad, aunque sea de pasada, remencionar las sustancias.
Tipos de energía que se almacena en moléculas orgánicas
Las así llamadas, son cuerpos formados por moléculas idénticas, entra las cuales pueden o no existir enlaces químicos. Veremos varios ejemplos. Las sustancias como el oxígeno, cloro, metano, amoníaco, etc., se presentan en estado gaseoso en condiciones ordinarias de presión y temperatura. Para su confinamiento se embotellan, aunque existen casos en que se encuentran mezcladas en el aire (os podéis dar una vueltecita por el Polo químico de Huelva).
En cualquier caso, un gas como los citados consiste en un enjambre de las moléculas correspondientes. Entre ellas no se ejercen fuerzas, salvo cuando colisionan, lo que hacen con una frecuencia que depende de la concentración, es decir, del número de ellas que están concentradas en la unidad de volumen; número que podemos calcular conociendo la presión y temperatura de la masa de gas confinada en un volumen conocido.

Decía que no existen fuerzas entre las moléculas de un gas. En realidad, es más exacto que el valor de esas fuerzas es insignificante porque las fuerzas residuales de las electromagnéticas, a las que antes me referí, disminuyen más rápidamente con la distancia que las fuerzas de Coulomb; y esta distancia es ordinariamente de varios diámetros moleculares.
Podemos conseguir que la intensidad de esas fuerzas aumente tratando de disminuir la distancia media entre las moléculas. Esto se puede lograr haciendo descender la temperatura, aumentando la presión o ambas cosas. Alcanzada una determinada temperatura, las moléculas comienzan a sentir las fuerzas de Van der Waals y aparece el estado líquido; si se sigue enfriando aparece el sólido. El orden crece desde el gas al líquido, siendo el sólido el más ordenado. Se trata de una red tridimensional en la que los nudos o vértices del entramado están ocupados por moléculas.
Todas las sustancias conocidas pueden presentarse en cualquiera de los tres estados de la materia (estados ordinarios y cotidianos en nuestras vidas del día a día).
Si las temperaturas reinantes, como decíamos en páginas anteriores, es de miles de millones de grados, el estado de la materia es el plasma, el material más común del Universo, el de las estrellas (aparte de la materia oscura, que no sabemos ni lo que es, ni donde está, ni que “estado” es el suyo).
En condiciones ordinarias de presión, la temperatura por debajo de la cual existe el líquido y/o sólido depende del tipo de sustancia. Se denomina temperatura de ebullición o fusión la que corresponde a los sucesivos equilibrios(a presión dada) de fases: vapor <-> líquido <-> sólido. Estas temperaturas son muy variadas. Por ejemplo, para los gases nobles son muy bajas; también para el oxígeno (O2) e hidrógeno (H2). En cambio, la mayoría de las sustancias son sólidos en condiciones ordinarias (grasas, ceras, etc.)
Las sustancias pueden ser simples y compuestas, según que la molécula correspondiente tenga átomos iguales o diferentes. El número de las primeras es enormemente inferior al de las segundas.

El concepto de molécula, como individuo-físico y químico, pierde su significado en ciertas sustancias que no hemos considerado aun. Entre ellas figuran las llamadas sales, el paradigma de las cuales es la sal de cocina. Se trata de cloruro de sodio, por lo que cualquier estudiante de E.G.B. escribiría sin titubear, su fórmula: Cl Na. Sin embargo, le podríamos poner en un aprieto si le preguntásemos donde se puede encontrar aisladamente individuos moleculares que respondan a esa composición. Le podemos orientar diciéndole que en el gas Cl H o en el vapor de agua existen moléculas como individualidades. En realidad y salvo casos especiales, por ejemplo, a temperaturas elevadas, no existen moléculas aisladas de sal, sino una especie de molécula gigante que se extiende por todo el cristal. Este edificio de cristal de sal consiste en una red o entramado, como un tablero de ajedrez de tres dimensiones, en cuyos nudos o vértices se encuentran, alternativamente, las constituyentes, que no son los átomos de Cl y Na sino los iones Cl– y Na+. El primero es un átomo de Cl que ha ganado un electrón, completándose todos los orbitales de valencia; el segundo, un átomo de Na que ha perdido el electrón del orbital s.

Cuando los átomos de Cl y Na interaccionan por aproximarse suficientemente sus nubes electrónicas, existe un reajuste de cargas, porque el núcleo de Cl atrae con más fuerza los electrones que el de Na, así uno pierde un electrón que gana el otro. El resultado es que, la colectividad de átomos se transforma en colectividad de iones, positivos los de Na y negativos los de Cl. Las fuerzas electromagnéticas entre esos iones determinan su ordenación en un cristal, el ClNa. Por consiguiente, en los nudos de la red existen, de manera alternativa, iones de Na e iones de Cl, resultando una red mucho más fuerte que en el caso de que las fuerzas actuantes fueran de Van der Waals. Por ello, las sales poseen puntos de fusión elevados en relación con los de las redes moleculares.
Hablemos de cuerpos.

Me referiré en primer lugar a los que constituyen nuestro entorno ordinario, que sería todo el entorno que abarca nuestro planeta. En segundo lugar considerare los demás cuerpos y objetos del Universo. El análisis de muestras de esos diversos cuerpos ha puesto de manifiesto que, en función de la composición, los cuerpos pueden ser simples y compuestos. Los primeros son, precisamente, los llamados elementos químicos, a las que el insigne Lavoisier (conocido como padre de la Química), consideró como el último término a que se llega mediante la aplicación del análisis químico.
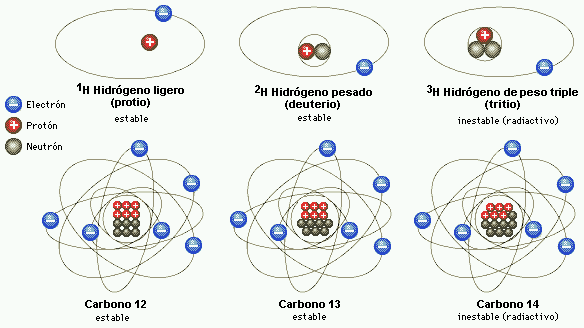
Hoy sabemos que son colectividades de átomos isotópicos.
La mayoría de ellos son sólidos y se encuentran en la Naturaleza (nuestro entorno terráqueo) en estado libre o en combinación química con otros elementos, formando los diversos minerales.
La ordenación de los iones en las redes se manifiesta externamente en multitud de formas y colores. No obstante, debo señalar que, aun siendo abundante esta variedad, no es tan rica como la que corresponde a los cuerpos vivos, tanto animales como vegetales. La explicación se basa en que el número de especimenes moleculares y su complejidad son mucho mayores que en el reino inorgánico.
Sería conveniente, salir al paso de una posible interpretación errónea. Me refiero a que pudiera pensarse que los reinos que acabamos de mencionar constituyen clases disyuntas, esto es, sin conexión mutua. Y no lo digo porque esté considerando el hecho de que el carbono forma compuestos inorgánicos y orgánicos (lo que también hace el silicio), sino porque haya existido, y aún pueda existir, una conclusión, mejor conexión evolutiva del mundo inorgánico y el viviente que no se puede descartar, de hecho, yo particularmente, estoy seguro de ello. Estamos totalmente conectados con los ríos, las montañas y los valles, con la tierra que pisamos, el aire que respiramos y con todo el resto del Universo del que formamos parte.

La teoría de Cairos Swith considera que el eslabón entre ambos mundos se halla localizado en los microcristales de arcilla. Mi teoría particular es que no hay eslabón perdido en dicha conexión, sino que es el tiempo el que pone, en cada momento, una u otra materia en uno u otro lugar. Ahora, nos ha tocado estar aquí como ser complejo, pensante y sensitivo. El eón que viene nos puede colocar formando parte de un enorme árbol, de un monte, o, simplemente estar reposando como fina arena en el lecho de un río. Sin dudarlo, J. M. y P. formarán parte de un hermoso jardín perfumado y lleno de aromas que la brisa regalará a los que pasen cerca de allí.
El granito, por ejemplo, consiste básicamente en una mezcla de tres cuerpos compuestos: cuarzo, mica y feldespato. ¿Quién puede decir hoy lo que seremos mañana?

En todos los cuerpos que hemos estado considerando hasta ahora, las moléculas, los átomos o los iones se hallan situados en los nudos de la correspondiente red, así que, los electrones de esos individuos se encuentran también localizados en el entorno inmediato de esos lugares. Podríamos decir que la densidad electrónica es una función periódica espacial, lo que significa que al recorrer la red siguiendo una determinada dirección irían apareciendo altibajos, es decir, crestas y valles de la densidad electrónica.
La estructura de los cuerpos metálicos, así como las aleaciones, merecen una consideración especial. La estructura de los metales y aleaciones difiere de la de los demás cuerpos en un aspecto muy importante que consideraré a continuación.

Supongamos, para fijar las ideas, que tenemos un trozo de plata metálica pura. En los nudos de la red correspondientes los átomos han perdido su electrón de …
Me refiero a que en los cuerpos metálicos existe una deslocalización de los electrones que están menos fuertemente enlazados en los correspondientes núcleos, es decir, de los electrones de valencia.
Vamos a precisar un poco. Supongamos, para fijar las ideas, que tenemos un trozo de plata metálica pura. En los nudos de la red correspondientes los átomos han perdido su electrón de valencia, pero ocurre que cada uno de estos electrones forma una colectividad que se halla desparramada o dispersa por todo el sólido. Una primera imagen de esta situación fue establecida por el gran físico italiano Enrico Fermi, por lo que se habla de un gas electrónico, llamado también de Fermi, que llenaría los espacios libres, es decir, no ocupados por los iones metálicos.
Este gas electrónico es el responsable de las propiedades metálicas, tales como el brillo, conductibilidades eléctrica y térmica, etc. La aplicación de la mecánica cuántica a la descripción del estado metálico conduce a la obtención del mapa de la densidad electrónica, o, como decía antes, a las características de la información correspondiente.
Sin entrar en detalles que desviarían nuestra atención hacia otros conceptos fuera de los límites de lo que ahora estoy pretendiendo, utilizaré el mismo lenguaje que para las estructuras de núcleos y átomos.

Recordemos que en la sociedad de los nucleones y electrones existen las relaciones verticales y las de estratificación, que se manifiestan en las capas y subcapas. En el caso de los metales tendríamos una colectividad de núcleos, arropados con sus capas cerradas, ocupando los nudos de la red; únicamente los electrones de valencia de cada átomo forman la colectividad del gas electrónico.
La pregunta que nos debemos hacer es: ¿estos electrones, en número igual, por lo menos, al de los átomos, se hallan estratificados? La respuesta es que sí. Existe una estratificación de estos electrones en las llamadas bandas. El concepto de banda energética resulta de la consideración simultánea de dos aspectos: la cuantización energética (o la estratificación de los niveles energéticos en los átomos) y el grandísimo número de electrones existentes. Este colectivo no podría ubicarse en un número finito y escaso de niveles. Esta dificultad queda soslayada si se admite que cada uno de esos niveles atómicos de los N átomos que forman el cuerpo se funde en otros tantos niveles de cierta anchura donde ya pueden alojarse los electrones disponibles.

Esa fusión de los niveles atómicos da lugar a las bandas. Esta imagen equivaldría a considerar un metal como un átomo gigante en el que los niveles energéticos poseyeran una anchura finita.
En cuanto a la información que puede soportar un metal, podríamos señalar que sería parecida a la del correspondiente átomo, pero mucha más extendida espacialmente. Una información puntual, la del átomo, daría paso a otra espacial, si bien vendría a ser una mera repetición periódica de aquella.
¿Y los cuerpos que pueblan el resto del Universo?
Cuando un cuerpo sobrepasa unas determinadas dimensiones, aparece algo que conocemos como fuerza gravitatoria y que se deja sentir en la forma que todos conocemos y, que da lugar, primeramente a la fusión de los diversos materiales que forman los cuerpos.
Así, por ejemplo, en el cuerpo que llamamos Tierra, la presión crece con la profundidad, por lo que, a partir de un determinado valor de ésta, aparece el estado líquido y con él una estratificación que trata de establecer el equilibrio hidrostático.
Dentro de nuestro sistema planetario se distinguen los planetas rocosos, hasta Marte y meteoritos inclusive, y el resto de ellos, desde Júpiter en adelante, incluido este. Estos últimos difieren esencialmente de los primeros en su composición. Recuérdese que la de Júpiter es mucho más simple que la de los planetas rocosos. Consta fundamentalmente de hidrógeno, helio, agua, amoniaco y metano, con un núcleo rocoso en su interior. El hidrógeno que rodea a este núcleo se encuentra en forma de hidrógeno atómico sólido.

También la composición del Sol (y todas las estrellas que brillan) es más simple que la de los planetas rocosos, su estado físico es el de plasma y su contenido está reducido (mayormente) a hidrógeno y helio. Mas variedad de materiales existe en las estrellas supernovas, donde el primitivo hidrógeno ha evolucionado de la manera que expliqué en otra parte de este trabajo.
En cuanto a los derechos de la evolución estelar, enanas blancas, estrellas de neutrones y agujeros negros, señalaré que la composición de la primera es sencilla en cuanto al numero de “elementos” constituyentes; la segunda ya lo indica su propio nombre, constan de nucleones, particularmente neutrones que están fuertemente empaquetados (muy juntos) por la gravedad. Una estrella de neutrones puede tener una densidad superior a la del agua, en millones de veces y del mismo orden que la de los núcleos atómicos. El agujero negro, es un fenómeno aparte, su inmensa fuerza gravitatoria es tal que, ni la luz puede escapar de ella, es decir, su velocidad de escape es superior a 300.000 km/s, y, como según la relatividad, nada es en nuestro Universo, superior en velocidad, a la luz, resulta que nada podrá escapar de un agujero negro.
Allí dentro, en el interior del agujero negro, no existen ni el tiempo ni el espacio, es como un objeto que estando en nuestro Universo (deja sentir su fuerza gravitatoria y engulle estrellas), al mismo tiempo, no está aquí. Son muchas las cosas que aún nos queda por dedcubrir.
emilio silvera
Ago
12
La Gran Nebulosa de Orion
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Orion ~
Clasificado en Orion ~
 Comments (0)
Comments (0)
Ciencia – ABC
La Gran Nebulosa de Orión, captada en una imagen con gran detalle
Es la región de formación de estrellas masivas más cercana al Sistema Solar. Por eso, estas nuevas observaciones permiten entender mejor cómo nacen las estrellas.

En el centro de la nebulosa las estrellas pueden ser hasta 30 veces más masivas y 200.000 veces más luminosas que el Sol – VLT
Investigadores han obtenido la primera imagen en alta resolución del borde de la nube molecular de Orión, la región de formación de estrellas masivas más cercana al Sistema Solar.
Los detalles de esta imagen, que permite estudiar la morfología y actividad que tiene lugar en la zona, se publican en la revista «Nature Letters», en un artículo que lidera el Consejo Superior de Investigaciones Científicas (CSIC).

La nebulosa de Orión es la región de formación de estrellas masivas más cercana y los astrofísicos la observan para estudiar el proceso de nacimiento y evolución de las mismas, que, en el caso del cúmulo del Trapecio -en el centro de la nebulosa-, llegan a ser hasta 30 veces más masivas y 200.000 veces más luminosas que el Sol.
Liderados por Javier Goicoechea, del grupo de Astrofísica Molecular del Instituto de Ciencia de Materiales de Madrid, los científicos consiguieron delimitar y estudiar con precisión la morfología y la actividad que ocurre en el borde iluminado de la nube (el interfaz donde sucede la transición entre el gas molecular frío y el gas atómico, ionizado y muy caliente), informa el CSIC.

Impresión artística que nos lleva en un viaje en 3D por la nebulosa de Orión. Crédito: ESO/M. Kornmesser. Enlace a vídeo original.
Esto fue posible gracias a la combinación de imágenes del borde de la nube Orión obtenidas con el observatorio ALMA (Atacama Large Millimeter/Submillimeter Array) y utilizando observaciones previas del telescopio VLT (Very Large Telescope), ambos en Chile.
«Hasta ahora teníamos una visión muy estática de lo que ocurre con el gas molecular en esa zona de transición debido a la poca precisión de los instrumentos. Eso ha cambiado radicalmente con ALMA», subraya Goicoechea.
Los datos obtenidos, añade, permiten lograr imágenes «con una sensibilidad exquisita» y con gran precisión; «prácticamente estamos fotografiando ‘la piel’ de Orión».
Filamentos en la nebulosa

«Las imágenes proporcionadas por ALMA revelan que el borde de la nube molecular está formado por pequeñas estructuras filamentarias y rugosidades con patrones periódicos», detalla el investigador.
Además de ser uno de los componentes «más fascinantes» de la galaxia, las «nubes moleculares» son el reservorio de material para formar nuevas estrellas.
Una de las preguntas que se hacen los investigadores es si estos grumos y filamentos densos observados podrían ser las «semillas» para la formación de una nueva generación de estrellas.
En este caso, la masa de los grumos detectados con ALMA en Orión es todavía muy pequeña comparada con la que se necesitaría para que la gravedad impulse su colapso y dé lugar a protoestrellas.
Para responder a si estos grumos pueden unirse en el futuro y dar lugar a condensaciones más masivas se necesitan más observaciones y modelos, lo que ayudará a entender si estos mecanismos que ocurren en «la piel» de Orión podrían ser un inductor de formación estelar, según Goicoechea.
Ago
12
Resuelto el misterio del neutrino estéril
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Astrofísica ~
Clasificado en Astrofísica ~
 Comments (0)
Comments (0)
Los datos de un Observatorio en la Antártida descartan casi por completo la posibilidad de que exista un neutrino que podría ayudar a explicar la materia oscura.
Los neutrinos son como los hobbits de la física de partículas. Prefieren estar en sus cosas, sin meterse en los líos políticos de los poderosos elfos o los ambiciosos humanos, y parecen insignificantes a su lado. Sin embargo, tienen algo, quizá fruto de esa autonomía respecto a otras partículas más poderosas, que les hace poder cambiar el mundo desde su posición aparentemente humilde.
Igual que un hobbit salvó a la Tierra Media del dominio del mal absoluto de Sauron, cuentan los físicos que pudieron ser los neutrinos quienes inclinaron la balanza hacia la antimateria en la lucha que se inició contra la materia en los orígenes del tiempo. Tras el Big Bang se había creado la misma cantidad de las dos sustancias y cada vez que una partícula con una carga chocaba contra su opuesta ambas se desintegraban dejando tras de sí un rastro de radiación. Si esa igualdad en la guerra hubiese perdurado, hoy no habría ni galaxias ni Tierra, ni humanos ni libros sobre hobbits.
Los neutrinos estériles podrían explicar por qué hay más materia que antimateria 
Como los hobbits, que se dividen en tres razas, los neutrinos se agrupan en tres sabores, asociados a otros tres leptones de distintas masas: el electrón, el muón y el tau. Estas partículas se crean cuando protones de alta energía, producidos en cataclismos cósmicos como las supernovas, chocan contra la atmósfera terrestre y desencadenan una lluvia de partículas diversas entre las que se encuentran los neutrinos. En su camino a través de la Tierra, fluctúan cambiando de sabor, un fenómeno cuyo descubrimiento fue premiado con el Nobel de Física en 2015.
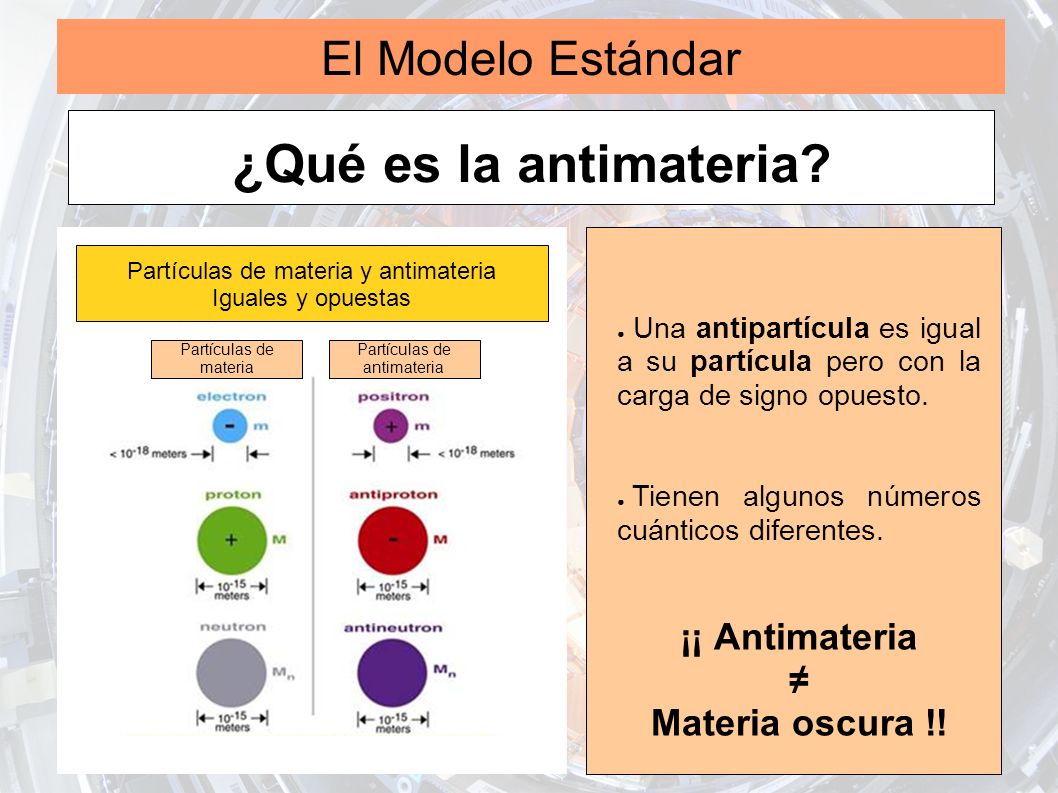
Estos hallazgos ya habían ayudado a reconfigurar el Modelo Estándar de física de partículas, que sirve para organizar nuestro conocimiento sobre cómo funciona la materia en su nivel más fundamental, pero en los últimos años, algunos científicos, a la vista de resultados experimentales difíciles de explicar con las partículas conocidas, habían planteado la posibilidad de que existiese un tipo de neutrino más. El neutrino estéril, como lo bautizaron, sería aún menos sociable que sus hermanos y solo trataría con el resto de la materia a través de la fuerza de gravedad. Su presencia habría ayudado a explicar si realmente los neutrinos desempeñaron un papel clave en el enfrentamiento entre materia y antimateria y podrían ayudar a entender qué es la materia oscura.
Sin embargo, un artículo publicado esta semana en la revista Physical Review Letters indica que tras mucho buscar no hay rastro de esta cuarta especie de neutrinos. Los autores llegan a esta conclusión después de analizar miles de neutrinos detectados por el Observatorio de Neutrinos IceCube del Polo Sur. Este particular telescopio está formado por 5.160 sensores congelados en el hielo antártico y distribuidos a una profundidad de entre 1,5 y 2,5 kilómetros en un espacio de un kilómetro cúbico. Esas dimensiones descomunales son necesarias para lograr atrapar las señales producidas por estas escurridizas partículas. Los neutrinos que intenta capturar IceCube se producen en la atmósfera sobre el Polo Norte y llegan a la Antártida después de atravesar toda la Tierra.

El telescopio IceCube cuenta con 5.160 detectores que ocupan un kilómetro cúbico bajo el hielo antártico
Los científicos esperaban que, si existiese, el neutrino estéril dejaría una señal clara en un determinado rango energético de un electronvoltio. Planteaban que este cuarto neutrino podría aparecer durante las fluctuaciones cuánticas que producen los cambios de sabor de la partícula. Pero esa señal no se ha encontrado. Además, los autores del trabajo han excluido la posibilidad de que se les haya escapado algo calculando la cantidad de neutrinos de cada clase generados en la atmósfera del Polo Norte. “Podemos detectar la cantidad de neutrinos muónicos, electrónicos y de tau y no hay nada que falte en la ecuación, así que la conclusión es que los resultados de IceCube debilitan la posibilidad de que este cuarto neutrino exista”, ha afirmado Jason Koskinen, investigador de la Universidad de Copenhague y coautor del estudio.

Este resultado es una muestra más de las posibilidades del telescopio de neutrinos antártico, una infraestructura que requirió una inversión de 271 millones de dólares. En noviembre de 2013, se publicó que durante los meses anteriores los detectores de IceCube habían atrapado 28 neutrinos procedentes de fuera del Sistema Solar. Entonces, los científicos anunciaron que la capacidad para detectar a aquellos mensajeros, capaces de viajar imperturbados por todo el espacio con información clave sobre la naturaleza del cosmos, como el hobbit que pudo entrar en Mordor sin ser detectado, abría una nueva era en la astronomía.
















 Totales: 87.472.947
Totales: 87.472.947 Conectados: 56
Conectados: 56























