Jul
29
Los átomos… Las estrellas… ¡Nuestra curiosidad!
 por Emilio Silvera ~
por Emilio Silvera ~
 Clasificado en Astronomía y Astrofísica ~
Clasificado en Astronomía y Astrofísica ~
 Comments (0)
Comments (0)
James Clerk Maxwell, el hombre sintiéndose poeta de la Naturaleza, inspirado escribió:
“En tiempos y lugares totalmente inciertos,
Los átomos dejaron su camino celeste,
Y mediante abrazos fortuitos,
Engendraron todo lo que existe.”
Y, al menos en lo que conocemos y que esté hecho de materia bariónica (la que emite radiación), así resulta ser. En la materia, de una u otra manera, están presentes las fuerzas fundamentales que rigen en el Universo, como por ejemplo, la radiactividad, la fuerza nuclear débil, la Gravedad y, en los átomos la fuerza nuclear fuerte.
- Radiación electromagnética.
- Radiación ionizante.
- Radiación térmica.
- Radiación corpuscular.
- Radiación solar.
- Radiación nuclear.
- Radiación de cuerpo negro.
- Radiación no ionizante.
TIPOS DE RADIACIÓN
- ALFA:
núcleos de Helio ( = 2 protones + 2 neutrones) - BETA: electrones
- GAMA: ondas electromagnéticas
El siglo XX fue el siglo nuclear: DE Curie a Merkel y de Becquerel a Fermi
Einstein no quiso participar en el Proyecto Manhattan
“Desde que se descubrió y hasta que fue utilizada con fines bélicos o para producir electricidad, la energía nuclear ha marcado las diferentes etapas del siglo xx. Una fuente de energía relativamente joven cuyo futuro se perfila muy difuso, a causa de los riesgos que plantea y de la corriente antinuclear que se reaviva cada día con más fuerza en la sociedad occidental.”
En los albores del siglo XX se hacía cada vez más evidente que alguna clase de energía “atómica” tenía que ser responsable de la potencia del Sol y las otras estrellas del cielo. Ya por 1898, sólo dos años después del descubrimiento de la radiactividad por Becquerel, el geólogo norteamericano Thomas Chrowder Chamberlin especulaba que los átomos eran “complejas organizaciones y centros de enormes energías”, y que “las extraordinarias condiciones que hay en el centro del Sol pueden… liberar una parte de su energía”. Pero nadie sabía cuál era ese mecanismo, ni cómo podía operar, hasta que no se llegó a saber mucho más sobre los átomos y las estrellas.

El intento de lograr tal comprensión exigió una colaboración cada vez mayor entre los astrónomos y los físicos nucleares. Su trabajo llevaría, no sólo a resolver la cuestión de la energía estelar, sino también al descubrimiento de una trenza dorada en la que la evolución cósmica se entrelazaba con la historia atómica y la estelar.
La clave para comprender la energía estelar fue, como previó Chamberlin, conocer la estructura del átomo. Que el átomo tenía una estructura interna podía inferirse de varias líneas de investigación, entre ellas, el estudio de la radiactividad: para que los átomos emitiesen partículas, como se había hallado que lo hacían en los laboratorios de Becquerel y los Curie, y para que esas emisiones los transformasen de unos elementos en otros, como habían demostrado Rutherford y el químico inglés Frederick Soddy, los átomos debían de ser algo más que simples unidades indivisibles, como implicaba su nombre (de la voz griega que significa “imposible de cortar”). Pero la física atómica aún debía recorrer un largo camino para llegar a comprender su estructura.
De los tres principales constituyentes del átomo -el protón, el neutrón y el electrón-, sólo el electrón había sido identificado (por J.J. Thomson, en los últimos años del siglo XIX). Nadie hablaba de energía “nuclear”, pues ni siquiera se había demostrado la existencia del núcleo atómico, y mucho menos de sus partículas constituyentes, el protón y el neutrón, que serían identificados respectivamente, por Thomson en 1913 y James Chadwick en 1932.
Rutherford con su experimento descubrió el núcleo atómico
Rutherford, Hans Geiger y Ernest Marsden se contaban entre los más expertos entendidos sobre la cartografía atómica. En Manchester, de 1909 a 1911, sondearon el átomo lanzando corrientes de “partículas alfa” subatómicas -núcleos de helio- contra delgadas laminillas de oro, plata, estaño y otros metales. La mayoría de las partículas alfa se escapaban a través de las laminillas, pero, para asombro de los experimentadores, algunas rebotaban hacia atrás, Rutherford pensó durante largo tiempo e intensamente en este extraño resultado; era tan sorprendente, señalaba, como si una bala rebotase contra un pañuelo de papel. Finalmente, en una cena en casa en 1911, anunció a unos pocos amigos que había dado con una expliación: que la mayoría de la masa de un átomo reside un un diminuto núcleo masivo. Midiendo las tasas de dispersión hacia atrás obtenida de laminillas compuestas de varios elementos, Rutherford pudo calcular la carga y el diámetro máximo del núcleo atómico del blanco. Esa era, pues, una explicación atómica de los pesos de los elementos. Los elementos pesados son más pesados que los elementos ligeros porque los núcleos de sus átomos tienen mayor masa.

El ámbito de los electrones fue explorado luego por el físico danés Niels Bohr, quien demostró que los electrones ocupan órbitas, o capas, discretas que rodean el núcleo. (Durante un tiempo Bohr concibió el átomo como un sistema solar en miniatura, pero este análisis pronto demostró ser inadecuado; el átomo no está regido por la mecánica newtoniana sino por la mecánica cuántica.) Entre sus muchos otros éxitos, el modelo de Bohr revelaba la base física de la espectroscopia. El número de electrones de un átomo está determinado por la carga eléctrica del núcleo, la que a su vez se debe al número de protones del núcleo, que es la clave de la identidad química del átomo.
Cuando un electrón cae de una órbita externa a una órbita interior emite un fotón. La longitud de onda de ese fotón está determinada por las órbitas partículas entre las que el electrón efectúa la transición. Y esta es la razón de que un espectro, que registra las longitudes de onda de los fotones, revele los elementos químicos que forman la estrella u otro objeto que estudie el espectros-copista. En palabras de Max Planck, el fundador de la mecánica cuántica, el modelo de Bohr del átomo proporciona “la llave largamente buscada de la puerta de entrada al maravilloso mundo de la espectroscopia, que desde el descubrimiento del análisis espectral había desafiado obstinadamente todos los itentos de conocerlo”.

Las estrellas son enormes aglomeraciones de gas, principalmente Hidrogeno, cuya temperatura es tan alta debido a la fusión de este elemento, que irradian luz a lo largo de todo el espectro electromagnético. Poseen diferentes temperaturas que varían desde los 2000 grados Celsius hasta los 50000.
De la misma forma que al calentar una pieza de metal cambia de color, al principio rojo, luego amarillo hasta llegar al blanco, el color de una estrella varia según su temperatura superficial. Las estrellas más frías son las rojas, y las mas calientes las azules. Estos colores suelen percibirse a simple vista, como por ejemplo Antares (la estrella principal de Scorpius) que es de color rojo, o Rigel (en Orion) de color azul. En astronomía se utiliza la escala Kelvin para indicar temperaturas, donde el cero absoluto es -273 grados Celsius.
Para definir el color de una estrella, Johnson y Morgan (1950), crearon el sistema UBV (del inglés Ultravioleta, Azul, Visible). Las mediciones se realizaban mediante un fotómetro fotoeléctrico para medir la intensidad de la radiación el longitudes de onda específicas:
- Ultravioleta: 3000 Å a 4000 Å
- Azul: 3600 Å a 5500 Å
- Visual: 4800 Å a 6800 Å
Con estos datos se pudo crear una serie de escalas: (B-V), (U-B) y (B-V). Cuanto mayor el número, más roja es la estrella. Para ver ejemplos de índices de color de diferentes estrellas, visite la sección de estrellas variables.
La tabla a continuación muestra el espectro electromagnético, con sus longitudes de onda.
Las escalas son las siguientes:
1 Å (Ångstron) = 1×10-8 cm (centímetros) = 1×10-10 m (metros)
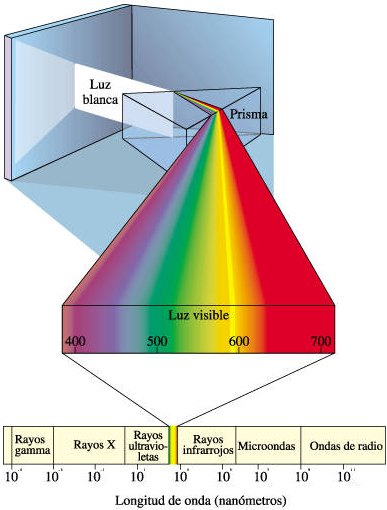
El ojo humano solo es capaz de percibir la pequeña porción que corresponde a la luz visible, situada entre los 3900 Å y 7500 Å, donde la menor se encuentra cerca del violeta y la mayor del rojo. El Sol emite en todas las longitudes de onda, pero solo llegan a la superficie una pequeña porción de estas, las demás son frenadas por la atmósfera: el ozono absorbe las mas altas longitudes de onda hasta el ultravioleta, y el vapor de agua absorbe gran parte de las infrarrojas.

En el Observatorio de la Universidad de Harvard, uno de los principales centros de la monótona pero prometedora tarea de la taxonomía estelar, las placas fotográficas que mostraban los colores y espectros de decenas de miles de estrellas se apilaban elante de “calculadoras”, mujeres , la mayoría, empleadas como miembros del personal de una facultad que les impedía asistir a clases u obtener un título.
Ella descubrió las primeras Cefeidas
Una de esas mujeres, Henrietta Leavitt (arriba), fue la investigadora pionera de las estrellas variables cefeidas que tan útiles serían a Shapley y Hubble, ella fue una de esas “calculadoras” de Harvard que, se encargaban de examinar las placas y registrar los datos en una pulcra escritura victoriana para su compilación en volúmenes como el Henry Draper Catalog, así llamado en honor al primer astrofotógrafo y físico que tomó las primeras fotografías del espectro de una estrella. Como presos que marcan el paso de los días en los muros de su celda, señalaban su progreso en totales de estrellas catalogadas. Antonia Maury, sobrina de Draper, contaba que había clasificado los espectros de más de quinientas mil estrellas. Su labor era auténticamente baconiana, del tipo que Newton y Darwin instaban a hacer pero raramente hicieron ellos, y las mujeres se enorgullecían de ella. Como afirmaba la “calculadora” de Harvard Annie Jump Cannon: “Cada dato es un facto valioso en la imponente totalidad”.
Precisamente fue Cannon quien, en 1915, empezó a discernir la forma de esa totalidad, cuando descubrió que la mayoría de las estrellas pertenecían a una de media docena de clases espectrales distintas. Su sistema de clasificación (ahora generalizado en la astronomía estelar), ordena los espectros por color, desde las estrellas O blanco-azuladas, pasando por las estrellas G amarillas como el Sol, hasta las estrellas rojas M. Era un rasgo de simplicidad debajo de la asombrosa variedad de las estrellas.

Pronto se descubrió un orden más profundo, en 1911, cuando el ingeniero y astrónomo autodidacto danés Ejnar Hertzsprung analizó los datos de Cannon y Maury de las estrellas de dos cúmulos, Las Híades y las Pléyades. Los cúmulos como estos son genuinos conjuntos de estrellas y no meras alineaciones al azar; hasta un observador inexperimentado salta entusiasmado cuando recorre con el telescopio las Pléyades, con sus estrellas color azul verdoso enredadas en telarañas de polvo de diamante, o las Híades, cuyas estrellas varían en color desde el blanco mate hasta el amarillo apagado.
Las Pléyades
Las Híades
Puesto que puede supònerse que todas las estrellas de un cúmulo están a la misma distancia de la Tierra, toda diferencia observada en sus magnitudes aparentes pueden atribuirse, no a una diferencia en las distancias, sino en las magnitudes absolutas. Hertzsprung aprovechó este hecho para utilizar los cúmulos como muestras de laboratorio con las que podía buscar una relación entre los colores y los brillos intrínsecos de las estrellas. Halló tal relación: la mayoría de las estrellas de ambos cúmulos caían en dos líneas suavemente curvadas. Esto, en forma de gráfico, fue el primer esbozo de un árbol de estrellas que desde entonces ha sido llamado diagrama Hertzsprung-Russell. Claro, como cabía esperar, la aplicabilidad del método pronto se amplió también a estrellas no pertenecientes a cúmulos.

Henry Norris Russell
(1877/10/25 – 1957/02/18)
Henry Norris Russell
Astrofísico estadounidense
Nació en el 25 de octubre de 1877 en Oyster Bay, Nueva York.
Henry Norris Russell, un astrofísico de Princeton con un enciclopédico dominio de su campo, pronto se puso a trabajar justamente en eso. Sin conocer siquiera el trabajo de Hertzsprung, Russell diagramó las magnitudes absolutas en función de los colores, y halló que la mayoría están a lo largo de una estrecha zona inclinada: el trondo del árbol de estrellas. El árbol ha estado creciendo desde entonces y hoy, está firmemente grabado en la conciencia de todos los astrónomos estelares del mundo. Su tronco es la “serie principal”, una suave curva en forma de S a lo largo de la cual se sitúan entre el 80 y el 90 por 100 de todas las estrellas visibles. El Sol, una típica estrella amarilla, está en la serie principal a poco menos de la mitad del tronco hacia arriba. Una rama más fina sale del tronco y se esxtiende hacia arriba y a la derecha, donde florece en un ramillete de estrellas más brillantes y más rojas: las gigantes rojas. Debajo y a la izquierda hay una cantidad de mantillo de pálidas estrellas entre azules y blancas: las enanas.

El Diagrama de Hertzsprung-Russell resumido
Este diagrama proporcionó a los astrónomos un registro congelado de la evolución, el equivalente astrofísico del registro fósil que los geólogos estudian en los estratos rocosos. Presumiblemente, las estrellas evolucionan de algún modo, pasan la mayor parte de su tiempo en la serie principal (la mayoría de las estrellas en la actualidad, en el brevísimo tiempo que tenemos para observar, se encuentran allí), pero empiezan y terminan su vida en alguna otra parte, entre las ramas o en el mantillo. Por supuesto, no podemos esperar para ver que esto sucede, pues el tiempo de vida, aun de estrellas de vida corta, se mide en millones de años. Hallar las respuestas exigirá conocer toda la física del funcionamiento estelar.
El progreso de la Física, mientras tanto, estaba bloqueado por una barrera aparentemente insuperable. Esto era literal: el agente responsable era conocido como la barrera de Coulomb, y por un tiempo frustó los esfuerzos de los físicos teóricos para comprender cómo la fusión nuclear podía producir energía en las estrellas…Pero eso, amigos, es otra historia que os contaré en otro momento.
emilio silvera
















 Totales: 67.065.436
Totales: 67.065.436 Conectados: 44
Conectados: 44























